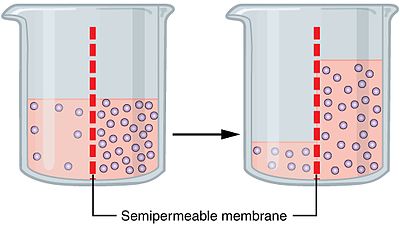
Osmoza je pasivni tok vode skozi polprepustno (semipermeabilno) membrano iz območja z nižjo koncentracijo topil (torej z višjo koncentracijo topila oziroma vode) v območje z višjo koncentracijo topil (nižjo koncentracijo topila). Ta premik zmanjša razlike v koncentracijah na obeh straneh membrane in se nadaljuje, dokler ni dosežena ravnotežna porazdelitev kemičnega potenciala vode. Osmoza ne zahteva neposrednega vnosa energije iz celice; giba se po gradientu kemičnega potenciala (termodinamičnemu nihanju proti nižjemu potencialu).
Mehanizem
Osmoza poteka, kadar membrana omogoča prehod topila (pogosto vode) ampak zadržuje večje topljence. S prostim prevajanjem so pomembni mikroskopski kanali v bioloških membranah, imenovani akvaporini, ki pospešijo prehod vode. Čeprav sama osmoza ne porabi ATP, je mogoče gibanje vode uravnavati s spremembo koncentracij topljencev ali z ustvarjanjem nasprotnega hidrostatičnega tlaka.
Osmotski tlak
Osmotski tlak je tlak, ki ga je treba povzročiti na stran z večjo koncentracijo topljenca, da se prepreči nadaljnje gibanje vode v to smer. Pri redkih raztopinah ga približno opisuje van 't Hoffov zakon: π = i·M·R·T, kjer je π osmotski tlak, i faktor disociacije, M molarna koncentracija topljenca, R plinska konstanta in T absolutna temperatura. V bioloških sistemih je osmotski tlak ključna količina, ker vpliva na volumen celic in hidrostatične sile v tkivih.
Pojmi: izoton, hipoton, hiperton
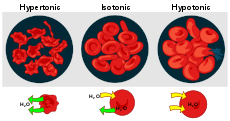
- Izotonične raztopine: koncentracija topljencev je enaka na obeh straneh membrane; ni neto toka vode.
- Hipotonična raztopina: zunanja raztopina ima manjšo koncentracijo topljencev kot notranjost celice; voda vstopa v celico — celica se lahko napihne ali celo razpoči.
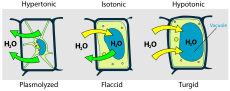
- Hipertonična raztopina: zunanja raztopina ima višjo koncentracijo topljencev; voda izstopa iz celice — celica se skrči (plazmoliza pri rastlinskih celicah).
Pomen v biologiji in vsakdanjih primerih
Osmoza igra ključno vlogo v številnih bioloških procesih:
- V rastlinah osmoza omogoča vnos vode skozi koreninske dlake in ustvarja turgor, ki podpira rastlinski tkivi.
- V živalih uravnavanje vode in ionov v celicah preprečuje ∗pretirano» nabrekanje ali skrčenje celic; krvne raztopine so prilagojene (izotonične), da ohranijo obliko eritrocitov.
- V medicini osmoza vpliva na delovanje ledvic in na metode, kot je dializa.
Praktične uporabe in tehnologije
Osmoza in njeni inverzni postopki imajo pomembne tehnološke aplikacije:
- Obratna osmoza: z uporabo tlaka, večjega od osmotskega, se voda potiska skozi membrano v nasprotni smeri — široko uporabljena metoda za razsoljevanje morske vode in čiščenje pitne vode.
- Prehrambena industrija: nadzor vlage in koncentracij pri konzerviranju ter pri sušenju živil.
- Farmacevtska industrija in laboratoriji: ločevanje snovi, priprava sterilnih raztopin in koncentracij.
Praktičen primer
Če postavimo jajce z odstranjeno lupino v čist vodo (hipotonično sredino), voda vstopa v notranjost jajca in ga napihne; če pa damo jajce v močno sladkorno ali slano raztopino (hipertonično), iz njega izteče voda in jajce se skrči. Podobno se obnašajo človeške celice: v hipotoniji lahko rdeče krvničke razpadejo (hemoliza), v hipertonični raztopini pa se skrumpljajo.
Kratka povzetek
Osmoza je temeljni pasivni proces prenosa vode preko polprepustnih membran, ki ga poganja razlika v koncentracijah topil. Osmotski tlak opisuje silo, potrebno za zaustavitev tega toka. Razumevanje osmoze je pomembno za biologijo, medicino, tehnologijo in industrijo, saj vpliva na ravnotežje tekočin v celicah in omogoča praktične postopke, kot je obratna osmoza za prečiščevanje vode.