Kemijska reakcija se zgodi, ko se ena ali več kemikalij spremeni v eno ali več drugih kemikalij. Primeri:
- železo in kisik se združita v rjo.
- kis in soda bikarbona se združita v natrijev acetat, ogljikov dioksid in vodo
- goreče ali eksplozivne stvari.
- številne reakcije, ki potekajo v živih bitjih.
- elektrokemične reakcije pri praznjenju ali polnjenju baterij.
Kaj se pri reakciji spremeni
Kemijske reakcije vključujejo prerazporeditev elektronov in preoblikovanje atomsko vezanih struktur. Atomi se med reakcijo ne spremenijo v druge elemente (to se zgodi le v jedrskih reakcijah), temveč se spremenijo le način in število vezi med njimi. Reakcijo pogosto zapišemo z reakcijsko enačbo, na primer:
2 H2 + O2 → 2 H2O
Pri zapisu je pomembna stohiometrija — ohranjanje mase in števila atomov v obeh členih enačbe.
Hitrost reakcij in dejavniki, ki jo vplivajo
Nekatere reakcije so hitre, druge počasne. Hitrost reakcije določa, kako hitro se reaktanti pretvorijo v produkte, in je odvisna od več dejavnikov:
- Temperatura: višja temperatura običajno pospeši reakcijo, saj delci imajo več kinetične energije in trčijo pogosteje in z večjo energijo.
- Koncentracija: večja koncentracija reaktantov poveča število trkov med delci in poveča hitrost reakcije.
- Površina stika: pri reakcijah, ki vključujejo trdne snovi, večja površina (na primer fino zdrobljen material) poveča hitrost.
- Katalizatorji: snovi, ki znižajo aktivacijsko energijo in pospešijo reakcijo, ne da bi se sami trajno porabili.
- Tlak in topilo: pri plinskih reakcijah povišan tlak in izbira topila pri reakcijah v raztopini lahko močno vplivata na potek.
Energija v kemijskih reakcijah
Pri nekaterih reakcijah se sprošča energija. To so eksotermne reakcije, pri katerih se proizvaja toplota (npr. zgorevanje), in lahko povzročijo dvig temperature okolice. Pri drugih reakcijah se energija sprejema. To so endotermičnereakcije, kjer reakcija potrebuje zunanji prispevek energije (npr. termoliza nekaterih spojin).
Energijske spremembe med reakcijami opisujemo z entalpijo (ΔH) in prostorsko s termodinamiko — reakcija je lahko kinetično počasna, a termodinamično ugodna ali obratno.
Glavne vrste kemijskih reakcij
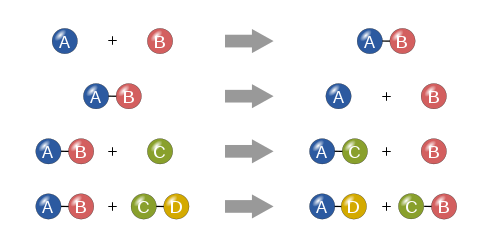
- Sinergijske (sintetne) reakcije: združevanje dveh ali več snovi v eno (A + B → AB).
- Razpadajoče (dekompozicijske) reakcije: razpad ene snovi v dve ali več (AB → A + B).
- Izmenjalne (zamenljive) reakcije: izmenjava atomov ali skupin med spojinami (AB + CD → AD + CB).
- Oksidacija–redukcija (redoks) reakcije: prenos elektronov med snovmi, kar vodi do sprememb oksidacijskih stanj (npr. rja železa).
- Kislinsko-bazične reakcije: prenos protonov (H+) med donatorjem in akceptorjem (npr. nevtralizacija kisline in baze).
- Prezcipitacijske reakcije: nastanek netopne snovi (padavine) pri mešanju dveh raztopin.
- Kompleksne reakcije in tvorba koordinacijskih spojin: vezava ligandov na ionske jedra.
- Elektrokemične reakcije: reakcije, pri katerih pride do pretoka elektronov skozi zunanji tokokrog (npr. v baterijah), kar je tudi primerirano v zgornjem seznamu.
Pomen kemijskih reakcij
Kemijske reakcije so osnova naravnih procesov in tehnologije: potekajo v celicah (presnova, fotosinteza), v industriji (proizvodnja gnojil, farmacevtikov, plastike), v energetiki (zgorevanje, baterije) in v vsakdanjih opravilih (kuhanje, čiščenje). Razumevanje reakcij omogoča nadzor nad njimi, varno ravnanje in razvoj novih materialov.
Varnost in nadzor
Ker nekatere reakcije sproščajo velike količine toplote, pline ali nastanejo strupene snovi, je pri eksperimentiranju ali industrijskem izvajanju nujno upoštevati varnostne ukrepe: ustrezno prezračevanje, zaščitno opremo, nadzor temperature in tlaka ter shranjevanje reaktantov.
Jedrske reakcije niso kemične reakcije. Kemijske reakcije vključujejo le elektrone v atomih, jedrske reakcije pa protone in nevtrone v atomskih jedrih. Jedrske reakcije spreminjajo jedra atomov in lahko sproščajo veliko več energije kot običajne kemijske spremembe.