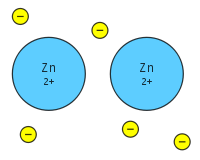
Kovinska vez je vrsta kemične vezi, pri kateri so valenčni elektroni delokalizirani in se ne vežejo na posamezen atom, temveč tvorijo skupno elektronsko "morje" okoli pozitivnih kovinskih ionov, katerih privlačnost elektronske gostote drži strukturo skupaj. Ta model pojasnjuje veliko značilnosti kovin in se razlikuje od kovalentne ter ionske vezi: medtem ko kovalentna vez temelji na delitvi parov elektronov med dvema jeder, ionska vez pa na elektrostatčni privlačnosti med nasprotnimi nabitostmi, kovinska vez temelji na kolektivni interakciji delokaliziranih elektronov in kovinskih jeder.
Mehanizem: delokalizacija in pasovna teorija
Kovinske vezi so posledica nizke ionizacijske energije kovinskih atomov, kar omogoča, da valenčni elektroni zapustijo posamezne atome in se prosto gibljejo po kristalni rešetki. Atomske orbitale sosednjih atomov se prekrivajo in tvorijo razširjene energijske pasove (valenčni in prevodni pas). Če so ti pasovi delno napolnjeni ali se medseboj prekrivajo, so elektroni prosti nosilci naboja in toplote.
Model "morja elektronov" poenostavljeno opisuje to situacijo: pozitivni ioni so potopljeni v oblak prostih elektronov, ki ustvarja močno privlačno silo med jedri in prostimi elektroni. Pasovna teorija pa daje kvantitativnejši opis energijskih stanj elektronov v trdni snovi in pojasnjuje prevodnost ter druge elektronske lastnosti kovin.
Ključne lastnosti kovin, ki izhajajo iz kovinske vezi
- Električna prevodnost: Ker so elektroni delokalizirani, kovine običajno dobro prevajajo električni tok — prosti elektroni hitro prenašajo naboj.
- Toplotna prevodnost: Prostori elektroni prenašajo energijo, zato kovine pogosto dobro prevajajo toploto (prevodnost toplote).
- Lesk: Interakcija prostih elektronov z vidno svetlobo povzroči značilen kovinski lesk.
- Plastičnost in duktilnost: Kovine se lahko deformirajo brez loma; znotraj elektronskega oblaka se atomi lahko premikajo (drsijo) drug mimo drugega, kar daje plastičnost in duktilnost.
- Mehanska trdnost in tališče: Močna privlačnost med kovinskimi ioni in delokaliziranimi elektroni daje kovinam značilno trdnost in pogosto visoka tališča ter vrelišča (čeprav se to razlikuje med različnimi kovinami).
- Spremenljive lastnosti: Lastnosti so odvisne od števila prostih elektronov, velikosti atomov in kristalne strukture — zato se lastnosti med kovinami močno razlikujejo.
Dejavniki, ki vplivajo na moč kovinske vezi
- Število valenčnih elektronov, ki so delokalizirani (več prostih elektronov običajno pomeni močnejšo vez).
- Velikost atomov in atomski polmer — manjši atom z enakim številom prostih elektronov pogosto začne močnejše privlačne sile.
- Kristalna struktura (npr. kubična ploščata, kubična zgoščena, heksagonalna zgoščena) vpliva na gostoto paketiranja in stabilnost vezi.
- Prisotnost d-elektronov pri prehodnih kovinah — d-orbitale lahko prispevajo k močnejšim vezem in večji trdnosti.
Izjeme in posebni primeri
Ne vse snovi z električno prevodnostjo so kovine. Nekateri nekovinski materiali prevajajo, ker imajo proste nosilce naboja: primer je grafit (ki ima, podobno kot kovine, delno delokalizirane π-elektrone vzdolž plasti). Tudi ionske spojine lahko prevajajo električni tok, kadar so stopljene ali raztopljene v vodi, ker so ioni prosti nosilci naboja.
Vse kovine nimajo povsem enake oblike kovinske vezi. Poseben primer je živega srebra (Hg2+
2) — nekatera Hg-olišča tvorijo kovalentne kovinsko-kovinske vezi in živo srebro je edina kovina, ki je pri standardnih pogojih tekoča zaradi kombinacije šibke kovinske vezi in relativističnih učinkov na valenčne elektrone.
Zlitine in vpliv na lastnosti
Zlitina je raztopina ali zmes kovin (včasih z majhnimi količinami nekovin) v trdnem stanju. Zlitine nastanejo z zamenjavo ali vpihovanjem atomov v kovinsko rešetko in s tem spreminjajo gostoto elektronskega oblaka in lokalno strukturo. Posledično zlitine pogosto pokažejo drugačne (običajno izboljšane) lastnosti, kot so večja trdnost, boljša odpornost proti koroziji ali spremenjena električna/termalna prevodnost. Mnoge zlitine so tudi bolj svetleče in uporabne v tehnologiji in industriji.
Dodatne opombe
- Prevodnost kovin se običajno z višanjem temperature zmanjšuje zaradi večjega razprševanja elektronov na termične vibracije rešetke; obstajajo pa kovine, ki pri zelo nizkih temperaturah postanejo superprevodne (preko ničelnega električnega upora).
- Kovinske vezi so v določenih primerih opisane tudi s kvantno-mehanskimi pristopi, ki natančno napovedo pasovno strukturo in gostoto stanj, kar je ključno za razumevanje elektronskih lastnosti materialov.
Povzetek: kovinska vez je kolektivna interakcija med pozitivnimi kovinskimi ioni in delokaliziranim elektronskim oblakom. Ta povezava pojasnjuje tipične kovinske lastnosti, kot so prevodnost, lesk, duktilnost in visoka trdnost, hkrati pa omogoča veliko variabilnost obeh lastnosti pri različnih kovinah in zlitinah.