Kovalentne vezi so kemijske vezi, kjer si dva ali več atomov (običajno nekovinska elementa) delita valenčne elektrone. Z združevanjem valenčnih elektronov atomi običajno dosežejo bolj stabilno elektronsko konfiguracijo (na primer okteto z osmimi elektroni v zunanji lupini, razen pri vodiku ali helija, ki sta stabilna z dvema elektronoma).
Nastanek kovalentne vezi — osnovna razlaga
Valenčni elektroni se ne gibljejo po klasičnih poteh, temveč so opisani z verjetnostnimi porazdelitvami oziroma orbitalami, kar določa kvantna mehanika. Ko se približata dva atoma z ohlapnima valenčnima elektronoma, se njune atomske orbitalne porazdelitve prekrivajo in nastaneta predvsem:
- vezujoča molekulska orbitala z nižjo energijo (v kateri je verjetnost najditve elektrona med obema jedroma večja),
- antivezujoča orbitala z višjo energijo (če je zasedena, zmanjšuje stabilnost vezi).
Prehod elektronov v nižjo (vezujočo) orbitalo pomeni sprostitev energije v okolico — to je razlog, da je tvorba vezi običajno energijsko ugodna. Energija, potrebna za razdor vezi, je približno enaka energiji, ki se sprosti pri njenem nastanku (to imenujemo energija vezi ali energija disociacije).
Elektronske lupine in valenčni elektroni
Število elektronov v atomu je enako številu protonov v jedru. Elektroni so razporejeni v plasteh (lupinah); prva lupina sprejme do dva elektrona, naslednje pa v mnogih primerih do osmih. Valenčni elektroni — torej elektroni v zunanji lupini — so tisti, ki sodelujejo pri tvorbi vezi. Kovalentna vez nastane, ko si atoma delita enega ali več parov valenčnih elektronov, kar poveča stabilnost obeh atomov.
Vrste kovalentnih vezi in lastnosti
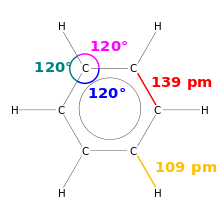
- Enojna, dvojna, trojna vezi: razlikujejo se po številu deljenih parov elektronov (eno-, dve- ali triodna vez) in po dolžini ter moči vezi (večvezi so običajno krajše in močnejše).
- Polarna in nepolarna kovalentna vez: če imata povezana atoma enako ali podobno elektronegativnost, je delitev elektronov skoraj enakomerna — vez je nepolarna. Če je en atom bolj elektronegativen, privlači elektronski oblak močneje, kar povzroči delne naboje (δ− in δ+) in polarnost vezi.
- Koordinativna (donska) vez: eden izmed atomov prispeva oba elektrona para za vez.
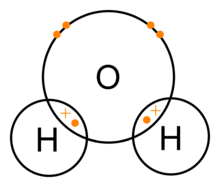
Primer: voda (H2O)
Molekula vode je sestavljena iz enega atoma kisika in dveh atomov vodika. Kisik ima v zunanji lupini šest valenčnih elektronov in za izpolnitev oktete tvori dve enojni kovalentni vezi — z vsakim vodikovim atomom si deli po en elektron. Vsaka od teh vezi je zato sestavljena iz para deljenih elektronov.
Ker je kisik bolj elektronegativno atom kot vodik, privlači deljene elektrone bolj k sebi. Posledica tega je, da ima kisik v molekuli vode majhen delni negativni naboj (δ−), vodik pa majhen delni pozitivni naboj (δ+). Ta neenakomerna porazdelitev elektronov povzroči, da je molekula vode polarna — njen električni naboj ni enakomerno porazdeljen.
Pomemben element polarnosti vode je tudi geometrija molekule: vezni kot O–H–O (natančneje kot H–O–H) je približno 104,5°, kar pomeni, da se vektorski učinki posameznih O–H dipolov ne izničijo, temveč se seštejejo v en skupni dipolni moment. Ta polarnost je osnova za številne lastnosti vode, kot so visoko površinsko napetost, dobro topilo za polarne snovi in sposobnost tvorbe vodikovih vezi med molekulami vode.
Zaključek — kaj si zapomniti
- Kovalentna vez pomeni delitev valenčnih elektronov med atomi in vodi k stabilnejši elektronski konfiguraciji.
- Vezuje se energija — pri tvorbi vezi se energija sprosti; pri prekinjanju vezi jo je treba vnašati (energija disociacije).
- Kadar imata atoma različni elektronegativnosti, vez postane polarna in nastopijo delni naboji (primer: voda, kjer je O δ− in H δ+).
- Razumevanje vezi zahteva kvantnomehanski opis orbital in molekulskih orbital, ne klasično “kroženje” elektronov po določenih poteh.