π (pi) vezi — definicija, lastnosti in pomen v kemiji
Pi (π) vezi — jasna definicija, fizikalne lastnosti, primeri in pomen v kemiji: nastanek, vpliv na reaktivnost, stabilnost in omejitve vrtenja molekul.
V kemiji so pi vezi (π vezi) kovalentne kemijske vezi, pri katerih se orbitalna pot enega elektrona križa (prekriva) s potjo drugega elektrona. Elektroni v pi vezi so skoncentrirani v dveh lobajah — nad in pod osjo vezi — zato govorimo o obliki, ki je pogosto opisana kot »osmice« okoli osi vezi. Obstajata dve območji prekrivanja (nad in pod osjo), medtem ko je vzdolž osi vezi navadno vozliščna ravnina z zelo malo elektronske gostote.
Kako nastane π vez
Pi vezi nastanejo s stranskim (»bočno«) prekrivanjem dveh atomskih p-orbital. Pomembne točke:
- Pi vez se oblikuje le, kadar sta p-orbitali orientirani vzporedno in se njihovi lobusi se dotikajo bočno — zato imata dve ločeni regiji prekrivanja (nad in pod osjo vezi).
- V primeru dvojne vezi je vez sestavljena iz ene σ (sigma) vezi in ene π vezi; pri trojni vezi sta ena σ in dve π vezi.
- Pri π vezih nastaneta tudi antibondingni orbital (π*), ki ima vozliščno ravnino med lobusi in višjo energijo kot vezni π orbital.
Lastnosti π vezi
- Pi vezi so običajno šibkejše od vezi sigma, ker je bočno prekrivanje p-orbital manj učinkovito kot glava-na-glavo (axialno) prekrivanje, ki tvori σ vezi. Kvantna mehanika pojasnjuje, da zaradi vzporedne orientacije orbital nastane manjša prekrivnost in zato manj vezne energije.
- Elektronska gostota v π vezi je razpršena izven jedrnega območja — ravno zato so π elektroni bolj dostopni za interakcije z reagentom ali z zunanjimi polji.
- Pi vezi omejujejo prostorno rotacijo okoli vezi: če bi molekula rotirala, bi se prekinitveno izgubilo vzporedno prekrivanje p-orbital in s tem π vez.
- Pi vezi imajo značilne vezne (π) in antivezne (π*) molekularne orbitale; prehodi elektronov med njimi (π → π*) so pogosto opazni v UV–Vis spektroskopiji.
Vez v molekulah — primeri in posledice
Tipični primeri π vezi so dvojne vezi v alkenih (npr. etilen C=C) in dve π vezi v trojnih vezeh (npr. acetilen C≡C). V aromatičnih spojinah, kot je benzen, so π elektroni delokalizirani nad več atomi, kar daje stabilnost skozi resonanco (aromatičnost).
- V molekulah z delokalizacijo (konjugirane sisteme) π sistemi znižajo energijsko vrzel med HOMO in LUMO, kar vpliva na barvila in UV–Vis absorpcijo.
- V aromatičnih spojinah so π elektroni razpršeni po obroču — to spreminja reaktivnost: aromatični obroči raje doživijo elektrofilno substitucijo kot elektrofilno adicijo, ker adicija poruši delokalizacijo π sistema.
Vloga v kemijski reaktivnosti in spektroskopiji
Pi elektroni so pogosto tarča elektrofilnih reagentov (npr. pri adicijah na alkene). Zaradi višje energije in večje dostopnosti kot σ elektroni so π vezi ključne v reakcijah, kot so:
- elektrofilna adicija alkenom,
- Diels–Alderove cikloadicije (reakcije konjugiranih dienov s štrene),
- nukleofilne adicije na aktivirane π sisteme in druge reakcije, ki izkoriščajo π* antibondingne orbite.
Spektroskopsko so π vezi pomembne pri:
- UV–Vis spektroskopiji (π → π* prehodi),
- IR spektroskopiji (značilni strižni in raztezni valovi C=C in C≡C),
- NMR spektroskopiji, kjer delokalizacija π elektronov vpliva na kemične premike (na primer aromatični pomiki).
π vezi in prehodne kovine, d–orbitali ter hipervalenca
Grška črka π v njihovem imenu označuje orbitale p. Simetrija orbital vezi π je podobna p orbitalam, če jih opazujemo po osi vezi. Pi vezi lahko nastanejo tudi z uporabo d orbital (npr. pri prehodnih kovinah ali pri hipervalentnih spojinah), čeprav je njihova prisotnost odvisna od energetskega soglasja orbital. Zamisli o veznih d orbitalah so pomembne pri razumevanju kompleksov in razširjenih vezav, vendar se mora vedno upoštevati relativna energija in prostorska orientacija orbital.
Povzetek
- Pi vezi so posledica bočnega prekrivanja p-orbital in tvorijo elektronsko gostoto nad in pod osjo vezi.
- So šibkejše od σ vezi, vendar igrajo ključno vlogo v reaktivnosti, delokalizaciji in spektroskopskih lastnostih molekul.
- Število π vezi določa red vezi (dvojna = ena π, trojna = dve π) in omejuje svobodno rotacijo okoli kovalentne vezi.
- V kompleksih s prehodnimi kovinami in v hipervalentnih spojinah lahko nastanejo tudi π interakcije z d orbitalami, kar razširi kemične možnosti vezave.
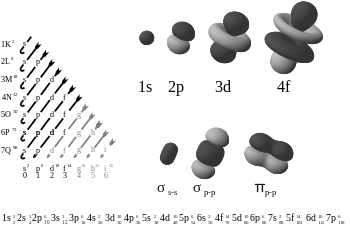
Elektronske atomske in molekulske orbitale, ki prikazujejo vez pi na spodnji desni strani slike.

Dve orbitali p, ki tvorita vez π.
Več vezi
Atomi, ki so povezani z dvojno vezjo, imajo eno vez sigma in eno vez pi. Če sta povezana s trojno vezjo, imata eno vez sigma in dve vezi pi.
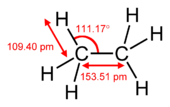
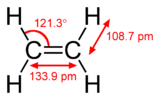
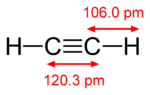
Vez pi je šibkejša od vezi sigma, vendar je kombinacija vezi pi in sigma močnejša od obeh vezi samih. Večja trdnost večkratne vezi v primerjavi z eno (vez sigma) se kaže na več načinov. Najočitnejši je zmanjšanje dolžine vezi. V organski kemiji so na primer dolžine vezi ogljik-ogljik v etanu (154 pm), etilenu (134 pm) in acetilenu (120 pm). Zaradi večjega števila vezi je skupna vez krajša in močnejša. Elektronska konfiguracija temelji na S, P, D in f-blokih. S ima 2 elektrona P ima 6 elektronov D ima 10 elektronov F ima 14 elektronov
|
|
|
|
| etan | acetilen |
Posebni primeri
Ni nujno, da se vezi pi povežejo s parom atomov, ki so prav tako povezani z vezmi sigma.
V nekaterih kovinskih kompleksih pi interakcije med kovinskim atomom in pi antivezavnimi orbitalami alkina in alkena tvorijo pi vezi.
V nekaterih primerih večkratnih vezi med dvema atomoma sploh ni vezi sigma, ampak samo vezi pi. Primeri so diiron heksakarbonil (Fe2(CO) 6), dikarbon (C ) 2in boran B 2H 2. V teh spojinah ima osrednja vez samo vez pi. Da bi dosegli čim večje prekrivanje orbital, so razdalje med vezmi veliko krajše od pričakovanih.
Vprašanja in odgovori
V: Kaj je v kemiji vez pi?
O: Vez pi je kovalentna kemijska vez, pri kateri se orbitalna pot enega elektrona križa s potjo drugega elektrona, pri čemer nastaneta dve območji prekrivanja, saj se poti prekrivata na obeh ploskvah.
V: Na katero grško črko se nanaša njihovo ime?
O: Grška črka v njihovem imenu je π in se nanaša na orbitale p.
V: Kakšna je orbitalna simetrija pi vezi?
O: Orbitalna simetrija vezi pi je videti enako kot orbitalna vez p, če jo gledamo po osi vezi, saj imajo orbitalne vezi p običajno takšno vezavo.
V: Zakaj so vezi pi običajno šibkejše od vezi sigma?
O: Vezi pi so običajno šibkejše od vezi sigma, ker so v skladu s kvantno mehaniko orbitalne poti vzporedne, zato se p-orbitale veliko manj prekrivajo.
V: Kdaj nastanejo vezi pi?
O: Vez pi nastane, ko se dve atomski orbitali stikata prek dveh območij prekrivanja.
V: Kaj so pi vezi?
O: Vezave pi so bolj razpršene vezi kot vezi sigma.
V: Ali se lahko molekularni deli, ki jih povezuje vez pi, vrtijo okoli te vezi, ne da bi prekinili vez pi?
O: Ne, molekularni fragmenti, ki jih povezuje vez pi, se ne morejo vrteti okoli te vezi, ne da bi prekinili vez pi, saj vrtenje uniči vzporedne poti dveh orbital p.
Iskati