Atom je osnovna enota snovi. Je najmanjša stvar, ki ima lahko kemijsko lastnost. Obstaja veliko različnih vrst atomov, vsak ima svoje ime, atomsko maso in velikost. Te različne atome imenujemo kemijski elementi. Kemijski elementi so razvrščeni v periodnem sistemu. Primera elementov sta vodik in zlato.
Atomi so zelo majhni, natančna velikost pa je odvisna od elementa. Atomi so široki od 0,1 do 0,5 nanometra. En nanometer je približno 100.000-krat manjši od širine človeškega lasu. Zato atomov brez posebnih orodij ni mogoče videti. Znanstveniki z eksperimenti ugotavljajo, kako delujejo in kako sodelujejo z drugimi atomi.
Atomi se združujejo v molekule: na primer dva atoma vodika in en atom kisika se združijo v molekulo vode. Ko se atomi združijo, se to imenuje kemijska reakcija.
Atomi so sestavljeni iz treh vrst manjših delcev, imenovanih protoni (ki so pozitivno nabiti), nevtroni (ki nimajo naboja) in elektroni (ki so negativno nabiti). Protoni in nevtroni so težji in se nahajajo v sredini atoma. Imenujeta se jedro. Obdaja jih oblak elektronov, ki so zelo lahki. Elektromagnetna sila jih privlači k pozitivnemu naboju jedra.
Število protonov in elektronov, ki jih ima atom, nam pove, kateri element je. Vodik ima na primer en proton in en elektron, element žveplo pa 16 protonov in 16 elektronov. Število protonov je atomsko število. Razen vodika ima jedro tudi nevtrone. Število protonov in nevtronov skupaj je atomska masa.
Atomi se v plinasti obliki gibljejo hitreje (ker se lahko prosto gibljejo) kot v tekoči ali trdni snovi. V trdnih snoveh so atomi tesno drug ob drugem, zato vibrirajo, vendar se ne morejo premikati (nimajo prostora), kot to počnejo atomi v tekočinah.
Sestava atoma in osnovne lastnosti
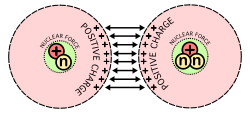
Jedro je zelo majhen, a zelo gost del atoma, ki vsebuje protone in nevtrone. Proton ima pozitiven naboj, nevtron nima naboja. Med protoni v jedru deluje močna jedrska sila, ki jih drži skupaj, kljub odbojni elektrostatni sili med pozitivnimi naboji.
Elektroni so negativno nabiti delci, ki okoli jedra zasedajo različne energijske plasti ali lupine (orbitele). Razporeditev elektronov določa kemične lastnosti atoma, zlasti število elektronov v zunanji lupini, imenovano valentni elektroni — ti odločajo o tem, ali bo atom tvoril vezi in katere vrste vezi (ionske, kovalentne, kovinske).
Izotopi in ioni
Izotopi so atomi istega elementa (enako atomsko število), ki se razlikujejo po številu nevtronov in s tem po atomski masi. Nekateri izotopi so stabilni, drugi radioaktivni in se s časom razpadajo.
Ioni nastanejo, ko atom izgubi ali pridobi elektrone. Pozitivni ion (kation) nastane ob odvzemu elektrona, negativni ion (anions) pa ob dodajanju. Ionske vezi največkrat nastopajo med kovinami in nekovinami.
Kemične vezi in molekule
Atomi tvorijo molekule, ko si delijo elektrone (kovalentna vez), izmenjujejo elektrone (ionska vez) ali delijo oblak elektronov (kovinska vez). Primer združitve: dva atoma vodika in en atom kisika tvorijo molekulo vode. Sestava in razporeditev elektronov določata, kako močno se atomi med seboj vežejo in kakšne lastnosti ima nastala snov.
Velikost, masa in merske enote
Atomske razdalje merimo v nanometrih ali pikometrih; tipičen atomski radij je reda 0,1–0,5 nanometra. Atomske mase se pogosto izražajo v atomski masni enoti (u ali Dalton). Pri večjih količinah snovi uporabimo Avogadrovo število (6,022×10^23) za pretvorbo med številom atomov in moli snovi.
Modeli atoma in zgodovina odkritij
Razumevanje atoma se je razvijalo skozi čas: John Dalton je v 19. stoletju predlagal idejo, da so snovi sestavljene iz nedeljivih delcev; J. J. Thomson je odkril elektron; Ernest Rutherford je pokazal obstoj majhnega jedra; Niels Bohr je uvedel kvantizirane orbite; sodobni kvantni model pa uporablja verjetnostne orbitalne oblike in kvantno mehaniko za opis elektronskega oblaka.
Kako znanstveniki preučujejo atome
Znanstveniki uporabljajo različne metode: spektroskopijo, pospeševalnike delcev, elektronsko mikroskopijo in skenirajoči tunelski mikroskop, ki omogočajo neposredno zaznavanje posameznih atomov ali njihovih učinkov. Z eksperimenti merijo lastnosti, kot so vezna energija, ionizacijska energija in elektronske orbite.
Atomi v različnih agregatnih stanjih
Hitrost gibanja atomov in prostorska ureditev se močno razlikujeta glede na agregatno stanje:
- V plinastem stanju se atomi ali molekule prosto gibljejo in trčijo med seboj.
- V tekočini so atomi v kontaktu, a se lahko premikajo drug okoli drugega, zato tekočine tečejo in imajo difuzijo.
- V trdni snovi so atomi tesno razporejeni in večinoma vibrirajo, vendar ne menjajo položajev, razen pri difuziji ali dislocacijah.
Pomen atoma v kemiji in vsakdanjem življenju
Razumevanje atomov je temelj kemije, fizike in biologije. Poznavanje atomske sestave snovi omogoča napovedovanje kemijskih reakcij, oblikovanje novih materialov, razumevanje biokemijskih procesov in razvoj tehnologij (npr. polprevodniki, zdravilne molekule, katalizatorji).
Če želite izvedeti več o osnovah snovi, kemijskih elementih ali primerih, lahko začnete pri pojmih, kot so kemijski elementi, atomsko maso in atomsko število, ali pa si ogledate konkretne primere, kot sta vodik in zlato.