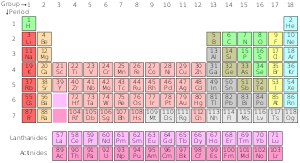
Periodni sistem kemijskih elementov je urejen seznam vseh znanih kemijskih elementov. V tabeli so elementi razporejeni po vrstnem redu atomskih števil, začenši z najmanjšim številom ena, vodik. Atomsko število elementa je enako številu protonov v jedru atoma in določa identiteto elementa. V periodnem sistemu so elementi razporejeni po periodah in skupinah. Vrstica v tabeli se imenuje perioda (številčena od 1 do 8). Prva perioda vsebuje le dva elementa: vodik in helij. Obdobji 2 in 3 imata po 8 elementov, daljše periode pa vsebujejo več elementov in vključujejo tudi prehodne elemente ter lantanoide in aktinoide. V vsaki periodi se elementi pojavljajo z naraščajočimi atomskimi števili.
Zgradba tabele in elektronska konfiguracija
Stolpec v tabeli se imenuje skupina. V standardnem periodnem sistemu je 18 skupin; vsaka ima svoje številčenje od 1 do 18. Elementi v isti skupini imajo sorodno razporeditev elektronov v zunanji (valenčni) lupini, zato imajo podobne kemijske lastnosti. Na primer, elementi z istim številom valenčnih elektronov pogosto tvorijo podobne spojine in reagirajo na podoben način. Skupina 18 so inertni plini ali žlahtni plini, ki zaradi popolnih zunanjih lupin reagirajo le redko.
Moderna razvrstitev temelji na elektronskih lupinah in nivojih ter deli tabelo na bloke (s, p, d, f), ki odražajo orbitale, ki se polnijo z elektroni. To razporejanje po blokih pomaga razumeti kemijsko obnašanje: npr. elementi s-bloka (skupini 1–2) so običajno zelo reaktivni kovinski elementi, medtem ko p-blok vsebuje širok spekter lastnosti od kovin do nekovin.
Glavne skupine elementov
- Skupina 1: alkalijske kovine — zelo reaktivne, mehke kovine (npr. cezij je zelo kovinski).
- Skupina 2: zemeljske alkalijske kovine — manj reaktivne od skupine 1, vendar še vedno tipično kovinske.
- Prehodni elementi (skupine 3–12): običajno kovine z več oksidacijskimi stanji, pomembne v industriji in kot katalizatorji.
- Skupina 17: halogeni — zelo reaktivne nekovine, tvorijo soli z alkalijskimi kovinami.
- Skupina 18: žlahtni plini — plini z zelo nizko reaktivnostjo zaradi polnih valenčnih lupin.
- Lantanoidi in aktinoidi: običajno so prikazani ločeno spodaj tabele; mnogi aktinoidi so radioaktivni in nekateri so sintetični.
Periodni zakon in zgodovina
Kemiki so periodni sistem uporabljali za prepoznavanje vzorcev in napovedovanje lastnosti neodkritih elementov. Zgodovinsko je pomemben prispevek dal ruski kemik Dmitrij IvanovičMendelejev (1834-1907), ki je v 19. stoletju uredil elemente po atomskih masah in napovedal lastnosti še neodkritih elementov; kasneje je postalo jasno, da je bolj temeljna vrednost za razvrščanje atomsko število (Moseley), kar je utrdilo sodobni periodni zakon. Leta 1990 je Mednarodna zveza za čisto in uporabno kemijo (IUPAC) sprejela enotno številčenje skupin z arabskimi številkami, ki je nadomestilo starejše sisteme, vključno z rimskimi številkami.
Periodični trendi in kemijske lastnosti
V periodnem sistemu se pojavljajo ponavljajoči se trendi, ki omogočajo napovedovanje lastnosti elementov:
- Atomski polmer: narašča navzdol v skupini (več elektronov in več lupin), zmanjšuje se z leve proti desni v periodi zaradi večjega pozitivnega naboja jedra.
- Ionizacijska energija: energija potrebna za odstranitev elektrona; običajno narašča levo→desno in zmanjšuje se navzdol.
- Elektronegativnost: sposobnost atoma, da privlači elektrone v vezi; narašča levo→desno in zmanjšuje navzdol (razen za žlahtne pline, kjer merjenje ni smiselno).
- Metaličnost: elementi pri dnu in levo tabele so najbolj kovinski, elementi zgoraj desno so nekovine. Metaloidi so v prehodni regiji med kovinami in nekovinami.
Posebnosti in sodobni vidiki
Več elementov, predvsem pri visokih atomskih številih, je sintetičnih in radioaktivnih; njihova stabilnost običajno upada z naraščajočim številom protonov. Periodni sistem se še naprej razvija z odkritji novih, prehodnih ali supertežkih elementov ter z izboljšanim razumevanjem jedrskih in kvantno-mehanskih učinkov. Element 101 je v čast Mendelejevu poimenovan mendelejev.
Uporaba periodnega sistema
Periodni sistem je ključno orodje v kemiji, fiziki, materialnih znanostih, biologiji in inženirstvu. Omogoča hitro primerjavo lastnosti elementov, ocenjevanje njihove reaktivnosti in izbiro primernih elementov za zlitine, katalizatorje, energetiko, medicino in druge tehnologije.
Z razumevanjem razporeditve elektronov, skupin in period ter periodičnih trendov lahko raziskovalci in študenti hitro predvidevajo vedenje elementov in načrtujejo kemijske reakcije ter nove materiale.