Elektronska konfiguracija je razporeditev elektronov v atomu. Povedano natančneje, elektronska konfiguracija opisuje, v katerih orbitalah se elektroni najverjetneje nahajajo in kolikšno je verjetnost njihove prisotnosti v okolici jedra. Zgradba periodnega sistema elementov delno temelji na razporeditvi elektronov po energijskih nivojih in podnivojih atomov.
Osnovne vrste orbital in njihove lastnosti
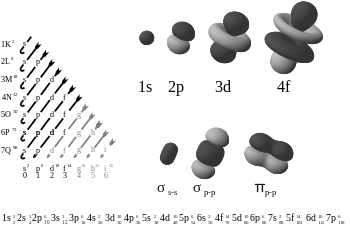
- s-orbitale: imajo sferično (kroglo) obliko. Vsaka s-podnivoin ima 1 orbitalo, ki sprejme največ 2 elektrona.
- p-orbitale: izgledajo kot par lopatic ali hanta (dve omogočeni regiji nasprotno od jedra). Vsak p-podnivoj ima 3 orbitalne (px, py, pz) in lahko sprejme skupaj do 6 elektronov.
- d-orbitale: imajo bolj zapleteno obliko (pogosto opisano kot štiriperesna deteljica ali z različnimi usmeritvami). D-podnivoj vsebuje 5 orbital in do 10 elektronov.
- f-orbitale: imajo zelo zapletene oblike (manj intuitivne za vizualizacijo) in skupaj 7 orbital, kar pomeni do 14 elektronov v f-podnivou.
Vsaka orbitala je matematična rešitev Schrödingerjeve enačbe za atom: predstavlja prostorsko porazdelitev verjetnosti, kjer lahko elektron obstaja. Pomembno je, da je vsaka orbitala v osnovnem stanju lahko zasedena z največ dvema elektrona, ki imata nasprotna spina.
Kvantna števila in konfiguracijska notacija
Elektronske konfiguracije se običajno zapisujejo z uporabo glavnih kvantnih števil (n), azimutalnega kvantnega števila (l) in števila elektronov v posameznem podnivoju. Pogosta notacija je n l^x (npr. 1s2, 2p4). Glavna načela:
- Kapaciteta: ena orbitala lahko sprejme do 2 elektronov; s-podnivoj = 1 orbitala (2 e-), p = 3 orbital (6 e-), d = 5 orbital (10 e-), f = 7 orbital (14 e-).
- Paulijevo izključitveno načelo: v istem atomu ne moreta biti dva elektrona z istima štirimi kvantnimi števili; posledično v eni orbitalu največ dva elektrona z nasprotnima spinoma.
- Hundovo pravilo: pri zasedanju degenerate orbital (npr. tri p-orbitale) najprej nastane čim več nepovezanih elektronov z istim spinom, preden se začnejo ustvarjati pari.
Zaporedje polnjenja (Aufbau in n + l pravilo)
Elektroni se v atomih običajno zasedajo orbitalo z najnižjo energijo najprej (Aufbau-princip). Poenostavljeno zaporedje energijskih podnivojev je:
1s < 2s < 2p < 3s < 3p < 4s < 3d < 4p < 5s < 4d < 5p < 6s < 4f < 5d < 6p < 7s ...
To zaporedje je posledica kombinacije glavnega kvantnega števila n in orbitalnega kvantnega števila l; pogosto se uporablja n + l pravilo za napoved relativnega vrstnega reda (nižji n + l pomeni običajno nižjo energijo; pri enakem n + l ima prednost nižje n).
Praktični primeri in izjeme
Primeri zapisa elektronskih konfiguracij:
- Vodnik (H): 1s1
- Helij (He): 1s2
- Oksigen (O): 1s2 2s2 2p4
- Železo (Fe): [Ar] 4s2 3d6 (pogosta zapisana oblika)
Obstajajo tudi znane izjeme pri prehodnih elementih zaradi stabilnosti polnih ali polopolnih d-podnivojev. Primeri:
- Krom (Cr): pričakovano [Ar] 4s2 3d4, dejansko pa pogosto [Ar] 4s1 3d5 (stabilen polpopoln d-podnivoj).
- Baker (Cu): pričakovano [Ar] 4s2 3d9, dejansko pa pogosto [Ar] 4s1 3d10 (stabilen poln d-podnivoj).
Pomen elektronskih konfiguracij
- Kemijske lastnosti: Elektronska konfiguracija določa valentne elektrone, ki odločajo o vezavnosti, oksidacijskih stanjih in reaktivnosti elementa.
- Periodni zakon: Ponavljajoče se lastnosti v periodnem sistemu so posledica podobnih konfiguracij valenčnih elektronov v elementih iste skupine.
- Spektroskopija in atomistične meritve: Energijske razlike med orbitalami se odražajo v absorpciji/emitiranju svetlobe (spektri), kar omogoča identifikacijo elementov in stanj elektronov.
- Magnetizem: Prisotnost nepovezanih elektronov vodi v paramagnetizem, popolnoma pari elektroni pa taro diamagnetizem.
- Kemične vezi: Oblika in energija orbital vplivata na orientacijo vezi in vrsto tvorjenih vezi (σ, π ...).
Dodatne opombe
Pomembno je razumeti, da ima vsak atom neomejen nabor možnih orbital v višjih energijskih stopnjah (tudi vodik), vendar so v osnovnem stanju zasedene le tiste z najnižjo energijo. Orbitalna teorija je kvantno-mehanska razlaga porazdelitve elektronov, zato so orbitalni prikazi vedno verjetnostne gostote in ne trde krožnice ali tirnice elektronov.
Ključno: znanje o elektronskih konfiguracijah je temelj razumevanja kemije in fizike atomov, zato so osnovna načela (Aufbau, Pauli, Hund) uporabna za napovedovanje obnašanja elementov in njihovo medsebojno povezovanje.