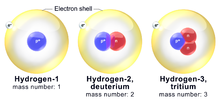
Atomi kemijskega elementa so lahko različnih vrst — te različice imenujemo izotopi. Izotopi imajo enako število protonov (in elektronov), torej enako atomsko število, vendar se razlikujejo po številu nevtronov in zato po masnem številu. Zaradi različnega števila nevtronov imajo izotopi istega elementa različne mase — z besedo masa mislimo, koliko snovi ali materije nekaj vsebuje.
Atomsko število, masno število in zapis izotopov
Atomsko število določa identiteto elementa (število protonov). Masno število (A) je vsota protonov in nevtronov v jedru. Izotopa istega elementa imata isto atomsko število, različni pa imata različna masna števila zaradi razlike v številu nevtronov. Izotop se pogosto zapiše kot AZX ali preprosto zimenzijsko, npr. 12C in 14C, kjer je zgornji indeks masno število.
Kemijske in fizikalne lastnosti
V nevtralnem atomu je število elektronov enako številu protonov, zato imajo izotopi istega elementa enako elektronsko konfiguracijo in so kemijsko zelo podobni. Ker pa se fizikalne lastnosti, kot je masa jedra, razlikujejo, se izotopi obnašajo fizično drugače — na primer imajo različne gostote, tališča ali hitrosti difuzije.
Masni učinek in kinetični izotopni učinek
Težji izotopi pogosto reagirajo nekoliko počasneje kot lažji izotopi istega elementa — to imenujemo masni učinek ali kinetični izotopni učinek. Ta učinek je najbolj opazen pri zelo lahkih elementih, na primer pri vodiku: prociju (1H) in devteriju (2H), saj ima devterij približno dvakrat večjo maso kot procij. Pri težjih elementih je relativna razlika med atomsko maso izotopov manjša, zato so učinki običajno manj izraziti.
Stabilni in radioaktivni izotopi
Nekateri izotopi so stabilni — njihova jedra ne razpadajo. Drugi so radioaktivni (nestabilni) in s časom razpadejo, pri čemer oddajajo sevanje (alfa, beta, gama). Radioaktivni izotopi imajo pomembno vlogo v datiranju (npr. 14C), medicini (npr. 99mTc, 18F) in jedrski energiji (npr. 235U).
Primeri izotopov
- Vodik: procij (1H), devterij (2H) in tritij (3H).
- Ogljik: 12C (stabilen), 13C (stabilen), 14C (radioaktiven, uporaben za radiokarbonsko datiranje).
- Uran: 235U (cenjen v jedrskih reaktorjih), 238U (pogostejši, daljša razpolovna doba).
- Klor: mešanica izotopov povzroča naravno atomsko maso klora ~35,45 u (teženo povprečje).
Izotopi v naravi in povprečna atomska masa
V naravi se elementi pogosto pojavljajo kot zmesi več izotopov. »Atomska masa« zapisa v periodnem sistemu je običajno tehtano povprečje mas vseh naravnih izotopov elementa glede na njihovo relativno naravno obilje. Zaradi tega imajo nekateri elementi neceloštevilske vrednosti atomske mase (npr. klor ~35,45).
Merjenje, ločevanje in uporabe izotopov
Izotopne sestave merimo z metodami, kot je masna spektrometrija, ki loči jedra glede na razmerje masa/naelektrenost. Ločevanje izotopov se opravlja z različnimi tehnikami (plinska difuzija, centrifugiranje, kemijske metode) in je ključno za pridobivanje posebnih izotopov (npr. obogatitev 235U ali priprava deuterirane vode).
Glavne uporabe izotopov:
- Radiokarbonsko datiranje (arheologija, geologija) z 14C.
- Medicinska diagnostika in terapija (sledi, PET, radiofarmacevtiki).
- Okoljske in biokemijske študije z izotopnimi sledilci (izotopno označevanje).
- Jedrska energija (gorivo in reaktorji) ter študije jedrskih procesov.
- Geokemija in paleoklimatologija – izotopne frakcionacije pomagajo razumeti starost, izvor in pretekle klimatske razmere.
Zaključek
Izotopi so različice istega elementa, ki se razlikujejo po številu nevtronov in posledično po masi, vendar imajo enako število protonov in enako elektronsko konfiguracijo. Zaradi tega so kemijsko podobni, fizikalno pa pogosto različni. Razumevanje izotopov je v kemiji, fiziki, medicini, geologiji in industriji ključno za številne metode, od datiranja do medicinske diagnostike in jedrske tehnologije.