Model slivovega pudinga je bil zgodnji (in kasneje ovržen) model atoma, ki ga je leta 1904 predlagal J. J. Thomson, kmalu po odkritju elektrona, a pred odkritjem atomskega jedra. Thomson je skušal pojasniti, kako je atom nevtralen kljub prisotnosti negativno nabitih elektronov — domneval je, da mora v atomu obstajati tudi enakomerno porazdeljen pozitivni naboj. V njegovem modelu je bil ta pozitivni naboj razporejen kot zgoščen, kontinuiren medij ali prostor, v katerem so bili "vloženi" negativno nabiti elektroni; zato so model hitro poimenovali "model slivovega pudinga", kjer so elektroni primerjali s slivami v pudingu.
Glavne značilnosti modela
- Atom je predstavljal homogen, pozitivno nabit volumen (sfero) znotraj katerega so bili razporejeni elektroni.
- Elektroni so po Thomsonovem pojmovanju tvorili statične ali počasne gibajoče se konfiguracije, ki so z elektrostatičnimi silami ohranjale ravnotežje v pozitivnem ozadju.
- Model je pojasnjeval električno nevtralnost atomov in nekatera makroskopska električna vedenja, vendar ni temeljil na kvantnih načelih, temveč na klasični elektrodinamiki.
Prednosti in omejitve
Model je imel eno pomembno prednost: ponudil je preprost, fizičen način za združitev odkritega elektrona z idejo nevtralnega atoma. Hkrati pa je imel več resnih pomanjkljivosti:
- Ni pojasnil eksperimentalnih opažanj, povezanih z razprševanjem delcev na atomih, niti ni mogel zadovoljivo razložiti spektralnih črt atomov (npr. diskretnih vrst linij v atomski emisijski spektr).
- Klasična elektrodinamika je napovedovala, da bi se pospešeni elektroni v takšni konfiguraciji hitro oddajali energijo in spiralno padali v pozitivno ozadje — torej model ni zagotavljal stabilnosti atoma dolgoročno.
- Model je predvideval razporeditev pozitivnega naboja kot kontinuum, kar ni bilo skladno z naslednjimi eksperimentalnimi rezultati, ki so nakazali koncentracijo naboja v majhnem volumnu.
Eksperimentalna ovržba in dediščina
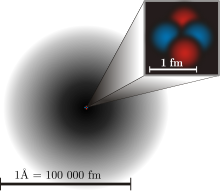
Konec desetletja po Thomsonovem predlogu so poskusi, predvsem Geiger–Marsdenovi poskusi (znani tudi kot Rutherfordov "zlatorazpršitveni" ali "gold foil" eksperiment, izvedeni pod vodstvom E. Rutherforda okoli leta 1909), pokazali, da velik del atomske mase in pozitivnega naboja ni razpršen kot homogeni medij, temveč je skoncentriran v majhni, gosto nabiti jedrni regiji. To je vodilo do Rutherfordovega jedrnega modela atoma (1911), pri katerem imajo elektroni orbite okoli majhnega pozitivnega jedra. Kasnejši razvoj — zlasti Bohrov kvantizirani model (1913) in splošnejši razvoj kvantne mehanike — je dokončno nadomestil Thomsonov prikaz kot napačen, a zgodovinsko pomemben korak.
Model slivovega pudinga je tako pomemben predvsem kot zgodnji poskus razlage strukture atoma v prehodnem obdobju med klasično fiziko in novo kvantno paradigmo. Pokazuje, kako so eksperimentalni dokazi (odkritje elektrona, kasneje razpršitveni eksperimenti) spodbujali postopno spreminjanje pojmov o notranji zgradbi materije.