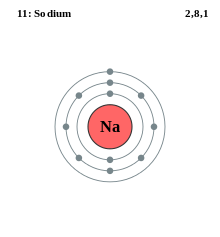
Elektronska lupina je zunanji del atoma okoli atomskega jedra. V njej so elektroni in je skupina atomskih orbital z enako vrednostjo glavnega kvantnega števila n. Elektronske lupine so osnovna sestavina elektronske konfiguracije atoma in določajo mnoge fizikalne in kemijske lastnosti elementov.
Struktura lupin in podlupin
Vsaka elektronska lupina vsebuje eno ali več elektronskih pod lupin ali podravni. Podlupine so sestavljene iz atomskih orbital, ki imajo enako vrednost orbitalnega kvantnega števila l. V posamezni podlupini je več orbital (ločljivost orbital je 2l+1), vsaka orbitala pa lahko sprejme največ dva elektrona z nasprotnima spinoma. Tako je skupno število elektronov v lupini enako 2 n 2 {\displaystyle 2n^{2}} 
Za praktične primere: lupina K (n = 1) lahko sprejme 2 elektrona, L (n = 2) do 8, M (n = 3) do 18 in N (n = 4) do 32 elektrone. Vendar pa pri dejanskih atomih zaporedje zapolnjevanja elektronov ne sledi vedno preprosto naraščajočemu n zaradi energijskih razlik med podlupinami (npr. 4s se običajno zapolni pred 3d).
Kvantna števila in vrste podlupin
- Glavno kvantno število n določa energijsko raven in približno razdaljo elektronov od jedra.
- Orbitalno kvantno število l določa obliko orbite in podlupino: s (l=0), p (l=1), d (l=2), f (l=3) itd.
- Magnetno kvantno število m_l določa orientacijo orbital v prostoru (od -l do +l).
- Spin kvantno število m_s (±1/2) določa spin elektrona v orbitalu.
Zapolnjevanje in pravila
V praksi se zapolnjevanje orbital ureja z naslednjimi načeli:
- Paulijev izključitveni princip: v isti orbitalni stanju sta lahko največ dva elektrona z nasprotnima spinoma.
- Aufbau princip: elektroni zapolnjujejo orbitala z nižjo energijo pred tistimi z višjo energijo (vodi v vrstni red, kot npr. 1s, 2s, 2p, 3s ...).
- Hundovo pravilo: pri zapolnjevanju več enakoenergijskih orbital (npr. tri p-orbitala) se elektroni razporedijo tako, da imajo največ neparnih spinov (maksimizacija skupnega spina) preden se začnejo pariti.
Vpliv na kemijske lastnosti
Valenčna lupina (zunanja delujoča lupina) določa prostorsko in energijsko razporeditev elektronov, ki sodelujejo v kemijskih vezavah. Število elektronov v valenčni lupini pojasnjuje reaktivnost elementov, tvorbo ionov in položaj elementa v periodnem sistemu. Poleg tega pojmi, kot so zaviralni (shielding) in efektivni jedrski naboj, pojasnijo, kako notranje lupine delno ščitijo zunanje elektrone pred privlačnostjo jedra, kar vpliva na atomski polmer, ionizacijsko energijo in elektronegativnost.
Spekterska notacija in izjeme
Elektronsko konfiguracijo pogosto zapisujemo v spektrski notaciji, na primer 1s2 2s2 2p6 za element neon. Pri nekaterih elementih, zlasti prehodnih kovinah in elementih z zapolnjenimi d- ali f-podlupinami, obstajajo izjeme od preprostega zaporedja zaradi stabilnosti polnih ali polpolnih podlupin (npr. konfiguracije pri Cr ali Cu).
Zgodovinski kontekst: Bohrov model
Ime elektronske lupine izhaja iz Bohrovega modela, po katerem naj bi se skupine elektronov gibale okoli jedra na določenih razdaljah, tako da njihove orbite tvorijo "lupine". Ta izraz je predstavil danski zdravnik Niels Henrik David Bohr. Bohrov model je bil pomemben zgodnji korak pri razumevanju atomske strukture, danes pa ga dopolnjuje kvantna mehanika, ki opisuje elektrone z verjetnostnimi gostotami in orbitalami namesto klasičnih krožnih poti.
Strnitev: elektronska lupina ni le fizična plast okoli jedra, ampak kvantno določena energijska raven, sestavljena iz podlupin in orbital, ki skupaj določajo elektronsko konfiguracijo atoma in njegove kemijske lastnosti.