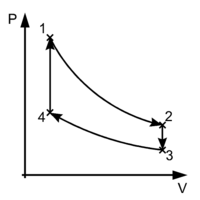
Termodinamični cikel je niz termodinamičnih procesov, ki sistem vrnejo v začetno stanje. Lastnosti so odvisne le od termodinamičnega stanja in se v ciklu ne spreminjajo. Spremenljivke, kot sta toplota in delo, v ciklu niso enake nič, temveč so odvisne od procesa. Prvi zakon termodinamike določa, da je neto dovedena toplota enaka neto opravljenemu delu v vsakem ciklu. Ponavljajoča se narava procesne poti omogoča neprekinjeno delovanje, zato je cikel pomemben pojem v termodinamiki.
Če se ciklični proces giblje v smeri urinega kazalca okoli zanke, je to toplotni motor in W bo pozitiven. Če se giblje v nasprotni smeri urinega kazalca, predstavlja toplotno črpalko in W bo negativen.
Načelo delovanja
Osnovna ideja termodinamičnega cikla je, da sistem skozi zaporedje procesov sprejme toploto iz enega vira, del dela preda okolici (ali porabi delo) in odvede preostalo toploto v drugi vir, pri čemer se ob koncu cikla povrne v začetno stanje. Na PV (tlak-volumen) diagramu je neto opravljeno delo enako površini, ki jo obdaja zanka cikla.
Zakoni in pomembne enačbe
- Prvi zakon (ohranjanje energije): ker je sprememba notranje energije ΔU v popolnem ciklu nič, velja Q_net = W_net. To lahko zapišemo tudi kot ∮δQ = ∮δW.
- Drugi zakon: določa smer pretočnega toka toplote in omejuje maksimalno uporabno delo, ki ga lahko pridobimo iz dane temperaturne razlike. Za reverzibilni (idealni) cikel med dvojnim toplotnim rezervoarjem je največja učinkovitost dana z izrazi za Carnotov cikel: η_C = 1 − T_c/T_h (temperaturi v kelvinih).
- Učinkovitost toplotnega motorja: η = W_out / Q_in = 1 − Q_out / Q_in. Višja kot je temperatura vira Q_in in nižja kot je temperatura odvodnega rezervoarja Q_out, večja je teoretična učinkovitost.
- Za črpalke in hladilnike: pomembni so koeficienti delovanja (COP): za hladilnik COP_R = Q_izhlajeno / W_in, za toplotno črpalko COP_HP = Q_oddano / W_in.
Vrste termodinamičnih ciklov
Obstajajo idealizirani in realni cikli, ki jih uporabljamo za različno tehnologijo. Najpogostejše skupine:
- Carnotov cikel (reverzibilni ideal): sestavljen iz dveh izotermičnih in dveh adiabatskih procesov; predstavlja zgornjo mejo učinkovitosti za motor med dvema temperaturnima rezervoarjema.
- Otto cikel: idealiziran cikel za bencinske (iskalne) motorje s stalnim volumnom pri vžigu; njegova učinkovitost je funkcija razmerja kompresije.
- Diesel cikel: model za dizelske motorje, pri katerem poteka vžig pri približno konstantnem tlaku; primeren za višje razmerje kompresije kot Otto.
- Brayton (Joule) cikel: ciklus za plinske turbine (npr. v letalskih motorjih); sestavljen je iz adiabatskega stiskanja, izotermičnega vstopa goriva/zgorevanja (približno konstantnega tlaka) in adiabatskega ekspanzije.
- Rankine cikel: klasični cikel parnih turbin (elektrarne); vključuje utekočinjenje pare in vmesno delo črpalke ter kotla.
- Cikli hladilnih naprav in črpalk toplote: (npr. obratni Rankine/paretni krogi, kompresijski hladilni cikli) — delujejo v obratni smeri kot motorji in za premik toplote porabijo delo.
Reverzibilnost, realne izgube in optimizacija
Idealni cikli (reverzibilni) dajejo zgornje meje učinkovitosti. V realnih napravah nastopijo izgube zaradi trenja, toplotnih izgub, nepopolnega zgorevanja, tlak- in temperaturnih padcev, nepopolne izmenjave toplote in notranjih neravnovesij. Ti dejavniki zmanjšajo dejansko učinkovitost v primerjavi z idealnimi modeli. Zato se v praksi uporabljajo tehnike, kot so regeneracija, rekuperacija, izboljšanje izolacije in optimizacija delovnih pogojev, da se izgube zmanjšajo.
Praktične uporabe
- Toplotni motorji: avtomobilski motorji (Otto, Diesel), plinske turbine (Brayton), parne turbine (Rankine).
- Hladilni sistemi in klimatske naprave: kompresijski in absorpcijski cikli.
- Toplotne črpalke: za ogrevanje prostorov z višjo energetsko učinkovitostjo kot neposredna električna ogrevanja.
- Industrialni procesi: kemična in elektrotermalna industrija uporablja cikle za prenos, shranjevanje in pretvorbo energije.
Povzetek: termodinamični cikel je temeljni koncept za razumevanje naprav, ki pretvorijo toploto v delo ali obratno. Ključno je razlikovati med stanji (ki določajo stanje sistema) in potmi/procesi (ki določajo količino toplote in dela). Učinkovitost cikla je omejena z zakoni termodinamike, zlasti z drugim zakonom, in v praksi dodatno zmanjšana zaradi različnih irreverzibilnosti.