Pentan je organska spojina s kemijsko formulo C
5H
12. Spada med alkane (splošna formula CnH2n+2, za n = 5) in vsebuje pet ogljikovih atomov. V splošni rabi z izrazom "pentan" pogosto označujemo vse tri ogljikove izomere iste bruto formule (n-pentan, izopentan in neopentan), vendar po IUPAC imenuje izraz pentan izključno linearni izomer, to je n‑pentan. Preostala dva izomera imata po IUPAC imeni 2‑metilbutan (pogosto imenovan izopentan) in 2,2‑dimetilpropan (pogosto imenovan neopentan). Kemijska formula ciklopentana je C
5H
10,, zato ni izomer pentana (ciklopentan ima namreč eno stopnjo nezasičenosti – obroč).
Izomeri pentana
Tri strukturne izomere pentana so:
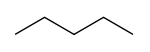
- n‑pentan (IUPAC: pentan) – linearna veriga: kondenzirana formula CH3–CH2–CH2–CH2–CH3; najpogostejši pomen besede "pentan" v splošnem govoru.
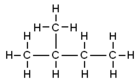
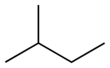
- 2‑metilbutan (pogosto: izopentan ali izoamyl) – razvejana veriga: CH3–CH(CH3)–CH2–CH3.
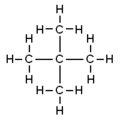
- 2,2‑dimetilpropan (pogosto: neopentan ali tetrametilmetan) – močno razvejan, kvartarni ogljik v središču: C(CH3)4 ali (CH3)4C.
Fizikalne in kemične lastnosti
- Molekulska masa: približno 72,15 g·mol−1.
- Stanje: pri sobni temperaturi so vsi trije izomeri brezbarvni, hlapni in vnetljivi tekočini (neopentan je pri zelo nizkih temperaturah lahko plin ali tekočina v odvisnosti od pogojev).
- Vretje (približno): n‑pentan ~ 36 °C, 2‑metilbutan ~ 28 °C, 2,2‑dimetilpropan ~ 10 °C. Razvejanost zniža vrelišče zaradi manjše površine stika med molekulami (manjše van der Waalsove sile).
- Topnost: praktično netopen v vodi, dobro topen v organskih topilih (eteri, ogljikovodikih, kloroformu itd.).
- Reaktivnost: kot nasičen ogljikovodik se obnaša kot tipičen alkan – relativno nizka kemijska reaktivnost, zgorevanje daje CO2 in H2O; lahko se uporablja v radikalnih substitucijah (halogeniranje) pri ustreznih pogojih.
Uporaba
- Pentan se uporablja kot razredčilo in organsko topilo v laboratorijih ter industriji.
- Je sestavina bencina in surovina v petrokemični industriji.
- V obliki nekaterih izomerov se uporablja kot hladilno sredstvo ali blowing agent pri proizvodnji poliuretanskih pen (zlasti n‑pentan v proizvodnji ekspandirane polistirenske pene).
Varnost in okoljski vpliv
- Pentan je zelo vnetljiv. Para z zrakom lahko tvori eksplozivne zmesi; zato ga je treba hraniti v dobro prezračenih prostorih, stran od virov vžiga in pri primerni temperaturi.
- Hitra inhalacija lahko povzroči omotico, omamljenost ali asfiksijo v primeru visokih koncentracij; dolgotrajni ali ponavljajoči stiki z visoko koncentracijo lahko vplivajo na osrednji živčni sistem.
- Je hlapna organska spojina (VOC) in prispeva k onesnaževanju zraka in tvorbi ozona v troposferi; ravnanje mora upoštevati okoljske predpise.
Za varno ravnanje upoštevajte tehnične listine (MSDS), lokalne predpise in navodila proizvajalca. Če potrebujete strukturne risbe, spektralne podatke ali natančne fizikalne konstante za posamezen izomer, jih lahko pripravim in navedem v nadaljevanju.