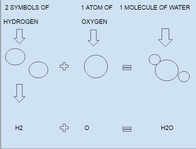
Kemijska formula je način, kako kemiki opišejo molekulo ali kemijsko spojino. V formuli je navedeno, kateri atomi so prisotni in v kakšnem številu. Včasih formula poda le sestavo (še posebej pri empiričnih in molekularnih formulah), včasih pa tudi način, kako so atomi med seboj povezani ali kako so razporejeni v prostoru (strukturne formule).
Črka označuje, kateri kemični element je posamezen atom. Pri tem velja pravilo pisave: prva črka simbolov elementov je velika, morebitna druga črka pa mala (npr. C za ogljik, Cl za klor). Spodnji indeks (subskript) kaže število atomov vsake vrste; če je prisoten le en atom določene vrste, subskript običajno izpustimo. Vodikov peroksid ima na primer formulo H2O2. Metan ima en atom ogljika (C) in štiri atome vodika; kemijska formula je CH4. Molekula sladkorja glukoza ima šest atomov ogljika, dvanajst atomov vodika in šest atomov kisika, zato je njena kemijska formula C6H12O6.
Vrste kemičnih formul
- Molekularna formula pokaže točno število vseh atomov v molekuli (npr. C6H12O6 za glukozo).
- Empirična formula poda najmanjše razmerje med atomi v spojini (npr. za vodikov peroksid H2O2 je empirična formula HO; za glukozo C6H12O6 pa je empirična CH2O).
- Strukturna formula prikaže povezanost atomov (vezave). Obstajajo polne Lewisove strukture, kondenzirane strukturne formule (npr. CH3CH2OH za etanol) in skeletne (opisne) formule, ki se pogosto uporabljajo v organski kemiji.
- Ionske formule izražajo razmerje med kationi in anioni v ioničnih spojinah (npr. NaCl, CaCO3 ali (NH4)2SO4).
- Hidrati vključujejo molekule vode, vezane v kristalni rešetki (npr. CuSO4·5H2O).
Pravila in oznake v zapisovanju
- Če je v formulah večkrat ponovljena skupina atomov, uporabimo oklepaje, npr. Ca(OH)2 ali (NH4)2CO3.
- Ko pišemo kemične enačbe, pred formule postavimo koeficiente za število molekul (npr. 2H2 + O2 → 2H2O).
- Za naboj ionov uporabljamo superskripte, npr. SO42−, Na+.
- Izotopno označevanje: izotop elementa z maso A se zapiše kot AElement (npr. 14C za radioaktivni ogljik-14).
Uporaba kemičnih formul
Kemijske formule so ključne pri opisovanju kemijskih enačb za opis kemijskih reakcij, pri določanju molskih količin, pri izračunu molarnih mas (seštevek atomskih mas posameznih elementov pomnoženih s števili atomov) in pri napovedovanju lastnosti spojin. Z njihovo pomočjo lahko tudi razlikujemo izomere — spojine z enako molekularno formulo, a različno strukturo in lastnostmi (npr. C2H6O: etanol in dimetil eter).
Primeri formul
- Voda: H2O
- Ogljikov dioksid: CO2
- Natrijev klorid (sol): NaCl
- Sumporna kislina: H2SO4
- Etilni alkohol (etanol), kondenzirana formula: C2H5OH ali CH3CH2OH
- Hidrat bakrovega sulfata: CuSO4·5H2O
Kratek zgodovinski pregled
Švedski kemik Jöns Jacob Berzelius je v 19. stoletju razvil ta sistem za zapisovanje kemijskih formul, ki je poenotil uporabo simbolov elementov in števčnih oznak. Danes so pravila zapisa dodatno standardizirana in razširjena, še posebej zaradi razvoja organskih in koordinacijskih formul ter računalniškega prikaza struktur.
Če želite izvedeti več o posameznih vrstah zapisov (strukturne formule, skeletni zapisi, računalniški formati) ali o izračunu molarne mase in uporabi formul v računskih primerih, lahko nadaljujemo z razširitvijo teh tem.