Drugi zakon termodinamike pravi, da se pri prehodu energije iz ene oblike v drugo ali pri prostem gibanju snovi entropija (nered) v izoliranem sistemu ne zmanjša — običajno se poveča ali ostane enaka pri idealno reverzibilnih procesih. Entropija je makroskopsko merilo za število mogočih mikro-stanj sistema in za razpršenost energije; v statistični mehaniki jo pogosto zapišemo kot S = k ln W, kjer je k Boltzmannova konstanta, W pa število mikro-stanj.
Termodinamično ravnovesje in prostorski gradienti
Razlike v temperaturi, tlaku in gostoti se čez čas vodoravno izenačijo zaradi toplotne prevodnosti, difuzije in mešanja — sistem teži k termo-dinamičnemu ravnovesju. V prisotnosti gravitacije pa lahko vztrajajo navpični gradienti: zaradi hidrostatičnega ravnotežja se tlak in gostota z višino spreminjata (na dnu sta običajno večja kot na vrhu) in se zato navpično ne izenačita.
Clausiusova in Kelvinova formulacija
Za eno najjasnejših formulacij drugega zakona je zaslužen Rudolf Clausius. Iz tega izhajajo tudi praktične izjave o usmerjenosti toplotnih procesov.
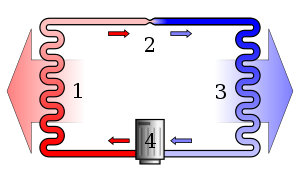
Toplota sama po sebi ne more prehajati s hladnejšega na bolj vroče telo.
Z drugimi besedami: brez opravil ali dela toplota ne teče proti višku temperature. Enakovredna izjava lorda Kelvina poudarja omejitev na pretvorbo toplote v delo:
Pretvorba, katere edini končni rezultat je pretvorba toplote, pridobljene iz vira pri konstantni temperaturi, v delo, je nemogoča.
Reverzibilnost, ireverzibilnost in omejitve učinkovitosti
Reverzibilen proces je idealizacija, pri kateri entropija sistema ostane nespremenjena; taka procesa so teoretična meja. Večina naravnih procesov je ireverzibilnih in povzroča povečanje entropije. Posledica tega so omejitve učinkovitosti toplotnih strojev: največjo teoretično učinkovitost toplotnega stroja, ki deluje med virom pri temperaturi Th in umivalnikom pri Tc, daje Carnotov izraz η = 1 − Tc/Th (temperaturi v Kelvinih). Noben resničen motor ne more preseči te meje.
Statistična razlaga in verjetnost
Drugi zakon je v osnovi verjetnostna: pove, kaj je zelo verjetno za sisteme z velikim številom delcev. V mikroskopskem smislu entropija meri število načinov, kako lahko sistem doseže isto makroskopsko stanje. Za velike sisteme so odstopanja od pričakovane rasti entropije izjemno malo verjetna, zato zakon drži praktično vedno. Pri majhnih sistemih se lahko pojavijo začasne fluktuacije, ki lokalno zmanjšajo entropijo.
Izolirani, zaprti in odprti sistemi
Pomembno je razlikovati med tipi sistemov: izoliran sistem ne izmenjuje energije ali snovi z okolico — drugi zakon se nanaša predvsem na takšne sisteme in pravi, da se njihova entropija ne zmanjša. Zaprti in odprti sistemi lahko zmanjšajo entropijo lokalno (na primer v živih organizmih ali hladilnikih), vendar to zahteva izmenjavo energije ali snovi z okolico in je vedno povezano s sorazmernim ali večjim povečanim entropije v okolici, tako da skupna entropija vesolja še vedno narašča.
Posledice za vsakdanje pojave in tehnologijo
- Toplota teče iz toplejšega telo v hladnejše (kava izhlapi in ohladi se v sobi).
- Ne moremo zgraditi stroja, ki bi pretvoril vso toploto iz enega vira neposredno v delo brez izpusta toplote v drugem delu sistema.
- Hladilni stroji in toplotne črpalke delujejo tako, da zunanji opravljeni del (ali proces zniževanja entropije) omogoča premik toplote iz hladnejšega v toplejše območje.
- Drugi zakon daje tudi časovno usmerjenost (»puščica časa«) — večina naravnih procesov poteka v smeri povečevanja entropije.
Primeri in opombe
Praktični primeri vključujejo mešanje plinov, ohlajanje vročega predmeta v hladnejšem okolju, izhlapevanje vode in delovanje toplotnih motorjev. Čeprav govorimo o »neredu«, je natančnejša interpretacija entropije v fiziki število mogočih mikro-stanj oziroma razpršenost energije — ne le kaos v običajnem pomenu besede.
Drugi zakon je temeljni zakon narave z obsežnimi posledicami v fiziki, kemiji, biologiji in inženirstvu. Velja z visoko gotovostjo za makroskopske sisteme; izjeme v obliki začasnih lokalnih zmanjšanj entropije so mogoče le pri majhnih sistemih in kot statistične fluktuacije.