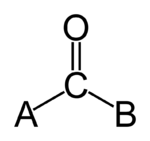
Karbonil označuje funkcionalno skupino C=O v molekuli — torej ogljikov (ogljikov) in kisikov (kisikov) atom, povezana z dvojno vezjo. Ogljik v karbonilu običajno oblikuje še dve drugi enovalentni vezi, ki sta lahko povezani z različnimi substituenti; primeri so karbonil v ketonu, aldehidu ali estru.
Struktura in elektronska porazdelitev
Kisik je bolj elektronegativen od ogljika, zato so elektroni dvojne vezi C=O pomaknjeni proti kisiku. To vodi v polarizacijo vezi: kisikov konec je delno negativen (δ−), ogljikov delno pozitiven (δ+). Kot posledica ima ogljik v karbonilu močne elektrofilske lastnosti in je dovzeten za nukleofilne napade.
Oba atoma v karbonilni skupini sta sp2 hibridizirana, vez in substituenti ležijo v istem ravninskem okolju, en π-elektronski pas pa tvori π-vez med C in O. Resonančni prispevek, pri katerem je kisik negativen in ogljik pozitiven, pojasnjuje reaktivnost in geometrijo skupine.
Glavne kemijske lastnosti in reakcije
- Nukleofilna adicija: Zaradi δ+ na ogljiku se pogosto izvede nukleofilni napad na ogljikov atom karbonila. To vodi do adicijskih produktov — na primer adicija hidrida (redukcija) ali alkoholnega oksidrila (nastanek hemicetalov in acetalskih derivatov).
- Redoks reakcije: Karbonili se lahko reducirajo v alkohole (npr. z NaBH4 ali LiAlH4). Aldehidi so tudi podvrženi oksidaciji v karboksilne kisline (npr. z Ag2O ali KMnO4), medtem ko so ketoni na splošno obstojnejši proti oksidaciji.
- Kondenzacijske reakcije: Karbonili reagirajo z drugimi nukleofili za tvorbo imina (z aminom), oksima (z hidroksilaminom), ali v aldolnih reakcijah ob medsebojni kondenzaciji med karbonili in njihovimi enolati.
- Enolizacija in reaktivnost α‑vodikov: Vodiki na α‑poziciji (ob karbonilu) so kisli in omogočajo nastanek enolatnih anionov, ki so ključni za reakcije, kot so aldolna kondenzacija, Michaelova adicija in alkilacije.
- Zaščita in derivatizacija: Karbonile je pogosto potrebno začasno zaščititi (npr. kot acetal), kadar želimo preprečiti njihove reakcije med zaporednimi koraki sinteze. Derivatizacija (npr. s 2,4‑DNP) se uporablja tudi za identifikacijo karbonilov.
Spektroskopske značilnosti
Karbonilna vez daje značilne in diagnosticne signale v različnih spektroskopskih tehnikah:
- Infrardeča spektroskopija (IR): močan in oster absorbcijski pas C=O običajno pri približno 1700 cm−1 (odvisno od vrste karbonila — aldehidi, ketoni, estri, amidi in karboksilne kisline se razlikujejo za nekaj deset cm−1 zaradi elektronsko‑steričnih učinkov).
- Spektroskopija NMR: signal ogljika karbonila v 13C NMR se pojavi pri visoki kemični premici (približno 160–220 ppm), zato je ločen od večine slabše ščepljivih signalov. Protonski NMR za aldehidne H‑atome se običajno nahaja pri okoli 9–10 ppm.
- UV/vis in masna spektrometrija lahko dodatno pomagata pri identifikaciji in določanju strukture karbonilnih spojin.
Primeri in pomen
Karbonilne spojine so prisotne v številnih naravnih snoveh (npr. kot ogljikovodični metaboliti, sladkorji v odprti obliki, steroidi) ter v mnogih zdravilih in drogah. So ključne v organski sintezi, saj omogočajo gradnjo kompleksnih ogljikovih ogrodij z vnosom novih veznih mest preko nukleofilne adicije ali kondenzacij.
Praktične metode za prepoznavanje
- Barvni testi: 2,4‑dinitrofenilhidrazin (2,4‑DNP) daje obarvane hidrazone z mnogimi karbonili; Tollensov test razlikuje aldehide (reducirajo Ag+) od ketonov.
- Spektroskopija: IR in NMR sta najhitrejši standardni metodi za potrditev prisotnosti C=O skupine.
Povzetek: Karbonilna skupina (C=O) je močno polarizirana, planarno usmerjena, elektrofilska funkcionalna skupina, ki omogoča številne organske reakcije — od nukleofilnih adicij in redukcij do kondenzacij in oblikovanja enolatov. Zaradi svoje reaktivnosti in široke razširjenosti ima ključno vlogo v kemiji, biokemiji in farmacevtski sintezi.