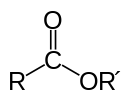
Ester je organska spojina, ki je derivat karbonilne skupine, kjer je na karbonilnem ogljiku vezana alkoksi (torej etrska) skupina. Splošna strukturna formula estrov je COOR (pogosteje zapisano R–COOR'), kar pomeni, da je vodik iz hidroksilne skupine karboksilne kisline nadomeščen z organsko skupino R'–O–.
Kako nastanejo esteri
Estri nastanejo na več znanih načinov. Najpogostejša pot v organski kemiji je Fischerjeva esterifikacija, torej reakcija karboksilne kisline z alkoholom v kislem okolju — v praksi to zapišemo kot karboksilna kislina + alkohol ⇄ ester + voda. Reakcija je reverzibilna in je pogosto v ravnotežju; za povečanje izhoda se uporablja odstranjevanje vode ali uporaba presežka enega reaktanta.
Poleg tega se esteri pripravljajo z vzpostavitvijo bolj reaktivnih karboksilnih derivatov, npr. reakcijo kislinskih kloridov ali anhidridov z alkoholi, ter z uporabo kondenzacijskih reagentov (npr. DCC) ali z metodi Steglichove esterifikacije — to so pomembne metode zlasti v sintezi farmacevtikov in peptidov.
Fizikalne in kemične lastnosti
- Esterske vezi vsebujejo polarno C=O skupino in C–O–C vez, vendar esteri običajno ne morejo delovati kot donorski H‑mostki (nima prostega O–H), zato imajo nižje vrelišča kot primerljive karboksilne kisline.
- Majhni esteri (npr. metil‑ in etil‑estri) so topni v vodi; z naraščajočo velikostjo ogljikovih verig topnost v vodi pade in topnost v organskih topilih narašča.
- Mnogi esteri imajo prijeten, pogosto sadni vonj in se zato uporabljajo v parfumih in aromah; maščobni esteri so glavna sestavina maščob in olj, kjer so običajno vezani v trigliceridih.
- Polimerizacija estrov diolov in dikarboksilnih kislin daje poliestre (npr. PET), ki so pomembni tehnični materiali.
Tipične reakcije esterov
Estri so aktivne pri različnih organkemičnih pretvorbah. Pomembne reakcije vključujejo:
- Hidroliza — v kislem okolju je reverzibilna (obrat Fischerjeve esterifikacije). V bazični okolici se esteri trajno razcepijo (saponifikacija) in tvorijo karboksilatne soli ter alkohol; to je osnovno načelo pri proizvodnji mil iz maščob.
- Transesterifikacija — izmenjava alkilne skupine na estru z drugim alkoholom; ta reakcija je osnova za pripravo biodizla (pretvorba trigliceridov v metilne estri maščobnih kislin).
- Redukcije — esteri se lahko reducirajo do alkoholov (npr. z LiAlH4) ali selektivno do aldehidov (z DIBAL‑H pri nizkih temperaturah). V določenih sintezah je možno iz estrov pridobiti tudi ketone, vendar običajno zahtevajo posebne reagente ali vmesne spojine (npr. Weinrebove amide) za nadzor stopnje acilacije.
- Nukleofilna acilna substitucija (adicija–eliminacija) — nukleofil napade karbonilni ogljik, tvori se tetraedrski vmesnik, nato izstopi alkoksid; to pojasnjuje reaktivnost esterov do različnih jedkih reagentov.
- Enolate in kondenzacije — esteri lahko tvorijo enolate in sodelujejo v reakcijah, kot je Claisenova kondenzacija, pomembni v izgradnji ogljikovih verig pri organski sintezi.
Spektroskopska in kemijska identifikacija
Estere lahko zaznamo in razlikujemo z več metodami:
- Infrardeča (IR) spektroskopija — daje značilen in relativno oster signal C=O pri približno 1735–1750 cm⁻¹ za alifatske estere (konjugacija ali aromatični sistemi premaknejo frekvenco). Poleg tega so prisotni signali C–O (≈1050–1300 cm⁻¹).
- Jedrska magnetna resonanca (NMR) — ogljikova NMR‑spektroskopija pokaže signal karbonilnega ogljika pri značilnih kemijskih premikih (običajno nižje kot pri ketonih/acidih); 1H NMR pogosto pokaže alkoksi protonske signale (npr. CH2–O pri ≈3,5–4,5 ppm), kar pomaga pri identifikaciji substituentov.
- Masna spektrometrija (MS) in fragmentacija lahko navedejo maso poleg fragmentov, značilnih za estere.
- Kemični testi — saponifikacija z NaOH ali CaO je klasična preiskava: nastanek soli karboksilne kisline potrdi prisotnost estrov.
Uporaba in primeri
Estri so v vsakdanjem življenju in industriji zelo razširjeni:
- Uporabljajo se kot sestavine parfumov in aroma (npr. izopentilacetat ima vonj po banani, etil butirat po ananasu).
- Veliko topil v industriji so esteri (npr. etilacetat) zaradi ugodnih topilnih lastnosti in hitro hlapnosti.
- V prehranski industriji so esteri običajno aroma‑snovi in aditivi; v naravi tvorijo sadne vonje.
- V materialni znanosti so iz esterov (kondenzacijskih reakcij med dikarboksilnimi kislinami in dioli) pridobljeni poliestri (npr. PET), uporabljeni v steklenicah, tekstilu in drugih plastnih izdelkih.
- Biodizel so tehnično metilni ali etilni estri maščobnih kislin, pridobljeni s transesterifikacijo rastlinskih olj ali živilskih maščob.
- V farmaciji so esteri pogosto uporabljen gradnik zdravil ali prodrugi, ki izboljšajo bio‑razpoložljivost zdravil.
Varnost in okolje
Mnogi esteri so relativno nestrupeni in biorazgradljivi, vendar so nekateri hlapni esteri vnetljivi in lahko povzročijo draženje dihal ali kože; zato je pri delu priporočena ustrezna ventilacija in zaščitna oprema. Maščobni esteri v naravi razgrajujejo encimi (lipaze), kar omogoča biološko razgradljivost maščob in olj v okolju.
Na kratko: esteri so vsestranska, kemično reaktivna in industrijsko zelo pomembna skupina organskih spojin, prisotna od naravnih maščob in eteričnih olj do plastike in topil; njihove lastnosti in pretvorbe omogočajo široko paleto uporab v kemiji in industriji.