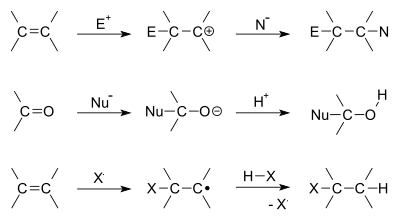
V organski kemiji se reakcija adicije zgodi, ko se dve molekuli združita in tvorita večjo molekulo. To se lahko zgodi le, če ima ena od molekul že dvojno ali trojno vez. To so lahko vezi ogljik-ogljik ali celo ogljik-kisik, ogljik-dušik in druge. Ena od obeh molekul se imenuje nukleofil in je tista, ki daje elektrone drugi molekuli, da nastane nova vez. Druga molekula se imenuje elektrofil in je tista, ki dobi elektrone.
Reakcija adicije je nasprotna reakciji eliminacije. Običajna primera reakcij adicije sta adicija vode na dvojno vez in nukleofilni napad na karbonil.
Kaj je adicija — razširjena definicija
Adicija je splošno ime za skupino reakcij, pri katerih reagenta pristopita k molekularnemu substratu in prekinejo π-vez ali drugo večkratno vez, da oblikujejo dve novi σ-vezi. Pogosta ciljna mesta so dvojne (C=C) in trojne (C≡C) vezi, pa tudi π-sistemi karbonilov (C=O) in konjugirane dvojnine. Adicije se lahko zgodijo z različnimi mehanizmi: elektrofilično, nukleofilno, radikalsko ali periciklično (npr. Diels–Alder).
Vrste adicijskih reakcij
- Elektrofilična adicija – tipična za alkene in alkinе. Elektrofil (npr. H+, Br+, Hg2+) najprej napade π-vez in tvori pozitivno nabit (ali delno nabit) vmesnik (npr. karbokation, bromonijev ion). Nato nukleofil napade ta vmesnik in dokonča adicijo. Primer: hydrohalogenation (HBr adicija na alkene).
- Nukleofilna adicija – značilna za elektrofilne π-sisteme, kot so karbonili (C=O). Nukleofil (npr. RO−, R−, H−, CN−) napade karbonilni ogljik in tvori alkoksidanion ali alkoksijonski vmesnik, ki se nato protonira. Primeri: dodajanje Grignard reagentov na aldehide/ketone, oblikovanje cijanohidrinov.
- Radikalska adicija – poteka prek prostih radikalov. Pogosta pri peroksid-iniciiranih reakcijah, npr. adicija HBr na alken v prisotnosti peroksidov vodi do anti-Markovnikovove selektivnosti.
- Periciklična adicija / cikloadicija – concerted (sinhrone) reakcije, kot je Diels–Alder, kjer se novo vezovanje zgodi preko cikličnega prehoda brez posrednih karbokationskih vmesnikov.
- Konjugirana (1,4) adicija – pri α,β‑nezasičenih karbonilih lahko pride do 1,2‑adicije (na karbonil) ali 1,4‑adicije (Michaelova adicija) na β‑ogljik; izbira je odvisna od nukleofila in pogojev.
Mehanizmi (podrobneje)
Običajni koraki elektrofilične adicije na alken so:
- 1) Elektrofilični napad na π-elektronski oblak, kar vodi do nastanka karbokationskega vmesnika ali cikličnega halogeniranega vmesnika (npr. bromonijev ion).
- 2) Nukleofilni napad na vmesnik iz bolj ali manj dostopne strani, kar določi stereokemijo (syn/anti) in regiokemijo.
Pri nukleofilni adiciji na karbonile nukleofil napade elektronsko osiščen karbonilni ogljik; nastali alkoksidanion se nato protonira, da da alkohol. Pri radikalski adiciji je pogosto prvi korak nastanek radikala (iniciacija), ki adira na dvojno vez in tvori nov radikal, nato pa se sledi propagacija in terminacija.
Regio- in stereokemija
- Markovnikovovo pravilo: pri adicijah protičnih reagentov (H–X) na nesimetrične alkenе proton običajno doda na ogljik z več vodikovi, elektrofilični napad vodi do bolj stabilnega karbokationskega vmesnika; nukleofil se nato veže na bolj substituirani ogljik. Izjeme so možne (npr. peroksidi za HBr — anti‑Markovnikov).
- Syn/Anti adicija: stereokemični izid je odvisen od mehanizma. Concerted adicije (npr. hidroboracija, Diels–Alder) pogosto dajo syn adicijo; adicije preko karbokationov lahko vodijo do racemizacije ali mešanih stereokemij; nastanek bromonijevega iona običajno vodi do anti adicije pri halogenacijah.
- Stereospecifičnost pri cikličnih sistemih: adicija na substituirane cikle lahko vodi do specifičnih cis/trans izomerov zaradi omejene rotacije in topoloških omejitev.
Pomembni primeri reagentov in reakcij
- Hidrogenacija (H2, Pd/C, Pt, Ni) — adicija H–H na C=C do saturacije.
- Halogenacija (Br2, Cl2) — anti adicija prek halogenonijevega iona.
- Hydrohalogenation (HCl, HBr, HI) — tvorba alkil halidov; regiokemija po Markovnikovu, razen če so prisotni peroksidi (anti‑Markovnikov pri HBr).
- Hidratacija (H2O z acid katalizo ali oxymercuration-demercuration) — pretvorba alkenov v alkohole; oxymercuration preprečuje rearrange in daje Markovnikov izdelek brez karbokationskega prehoda.
- Hidroboracija‑oksidacija (BH3/THF → H2O2, OH−) — daje anti‑Markovnikov alkohol z overall syn adicijo.
- Adicija nukleofilov na karbonile — Grignard reagenti (RMgX) ali organski litijevi reagenti (RLi) dajo alkohol po protoniranju; cianoformiranje (KCN) tvori cijanohidrine.
- Diels–Alder (4+2 cikloadicija) — sinhrona adicija diena in dienofila, pomembna metoda za tvorbo cikličnih struktur.
Pogoji, katalizatorji in kinetika
Adicije so lahko katalizirane z kislino (H+ ali Lewisove kisline, npr. BF3), bazo (pri nekaterih nukleofilnih adicijah), kovinskimi katalizatorji (hidrogenacije, metal‑katalizirane adicije) ali radikalnimi iniciatorji (peroksidi, AIBN). Kinetika in izid sta odvisna od stabilnosti vmesnikov (npr. karbokationov), topnosti reagentov in topokemije reaktantov.
Konjugirane sisteme in 1,2 vs 1,4 adicija
Pri α,β‑nezasičenih karbonilih (enoni) obstaja možnost napada nukleofila na karbonilni ogljik (1,2‑adicija) ali na β‑pozicijo (1,4 ali Michaelova adicija). Izbor je odvisen od vrste nukleofila (trdi nukleofili pogosto dajejo 1,2; mehkejši nukleofili in stabilizirane anione pogosto 1,4) in pogojev (topilo, temperatura, katalizator).
Polimerizacija kot ponavljajoča se adicija
Veliko polimerizacijskih procesov je vrste adicije, kjer monomeri (alkeni) dobesedno dodajajo drug na drugega, da tvorijo polimerni verigi (npr. polietilen, polipropilen). Mehanizmi vključujejo radikalsko, ionsko ali katalizirano koordinacijsko adicijo.
Pomen v organski sintezi
Adicije so temeljne transformacije v sintezi: omogočajo vnašanje funkcionalnih skupin, širjenje ogljikovih verig in hitro gradnjo zapletenih molekul. Izbira prave metode adicije (npr. hidridno reduciranje, Grignard, oxymercuration, hidroboracija) omogoča nadzor nad regiokemijo in stereokemijo produkta.
Varnost in okoljski vidiki
Mnogo reagentov za adicije (halogeni, peroksidi, močne kisline, kovinski katalizatorji) so strupeni, oksidativni ali vnetljivi; ravnanje zahteva ustrezne varnostne ukrepe in primerno odlaganje. Katalizirane H2 hidrogenacije so pogosto zelena možnost v primerjavi s stoikiometričnimi, vendar je pomembno upoštevati varnost pod tlakom in metalno kontaminacijo.
Zaključek
Reakcija adicije je širok pojem, ki vključuje različne mehanizme in aplikacije v organski kemiji. Razumevanje mehanizma, vmesnikov in pogojev omogoča racionalen izbor metode za dosego želene regiokemije in stereokemije v sintetičnih postopkih.