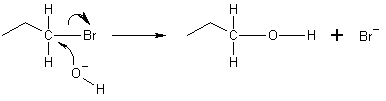
Nukleofil je vrsta, ki v reakciji odda elektronski par elektrofilu, da nastane kemijska vez. Vse molekule ali ioni s prostim elektronskim parom so lahko nukleofili. Ta par elektronov se imenuje osamljeni par. Ker nukleofili oddajajo elektrone, ustrezajo definiciji Lewisove baze. Nukleofili torej delujejo kot elektronski darovalci in napadajo dele molekul, ki imajo polni ali delni pozitivni naboj.
Atributi in pomen pojma nukleofilnost
Nukleofilna opisuje privlačnost nukleofila na jedra. Nukleofilnost, včasih imenovana moč nukleofila, se nanaša na sposobnost snovi, da napade elektrofil in tvori novo vez; pogosto se uporablja za primerjavo učinkovitosti različnih nukleofilov pri istih pogojih.
Faktori, ki vplivajo na nukleofilnost
- Električni naboj: negativno nabiti nukleofili (npr. OH−, CN−) so običajno bolj reaktivni kot njihovi nevtralni analogi (npr. H2O, NH3).
- Elektronegativnost: atom z nižjo elektronegativnostjo drži elektron bolj ohlapno in je pogosto bolj nukleofilen (npr. I− je v protitičnih topilih bolj nukleofilen kot F−).
- Polarizabilnost (velikost): večji, lažje polarizabilni ioni (npr. S- ali I−) lahko bolje oblikujejo začasne interakcije in so pogosto močni nukleofili v protitičnih topilih.
- Sterične ovire: prostorsko obremenjeni nukleofili (npr. tert-butiloksid) imajo zmanjšano nukleofilnost zaradi omejenega dostopa do elektrofilnega centra.
- Resonanca in konjugacija: delokalizacija osamljenega para zmanjša njegovo razpoložljivost za napad (npr. fenolatni ion je manj nukleofilen na aromatskem ogljiku, če je par delokaliziran).
Vpliv topila
Topilo močno vpliva na opazovano nukleofilnost. V protitičnih topilih (npr. voda, alkoholi) so majhni močno hidrirani ioni (npr. F−) manj reaktivni, ker jih obkrožajo molekule topila. V aprotitičnih topilih (npr. DMSO, acetone) so ti ioni manj hidrirani in torej močnejši nukleofili. Zato se vrstni red nukleofilnosti halogenidov spremeni glede na topilo:
- V protitičnih topilih: I− > Br− > Cl− > F−
- V aprotitičnih topilih: F− > Cl− > Br− > I−
Nukleofilnost vs. baznost
Čeprav sta pojma povezana (oba vključujeta razpoložljivost elektronskega para), se razlikujeta: baznost meri afiniteto do protona (H+), medtem ko nukleofilnost meri sposobnost napada na elektrofilski atom (npr. ogljik). V nekaterih primerih lahko spojina velja za močno bazo, a ne nujno za najboljši nukleofil (in obratno), še posebej v različnih topilih ali če sta pomembni sterika in polarizabilnost.
Vloga pri nukleofilnih substitucijah (SN1, SN2) in solvoliza
Nukleofili pogosto sodelujejo v reakcijah nukleofilne substitucije. Pri mehanizmu SN2 je hitrost reakcije neposredno odvisna od koncetracije in moči nukleofila — močnejši nukleofil povzroči hitrejši neposredni enostopenjski napad. Pri SN1 pa je počasnejši korak tvorba karbokationa; nukleofilnost običajno manj vpliva na hitrost, saj je ključen stabilnost prehoda (in molekularno okolje). Nevtralne nukleofilne reakcije s topili, kot so alkoholi in voda, se imenujejo solvoliza — v teh reakcijah topilo samo deluje kot nukleofil (npr. voda pri hidrolizi).
Primeri pogostih nukleofilov in njihova uporaba
- OH−, RO− (alkoksidi) — močni nukleofili, uporabljeni v deprotonacijah in SN2 reakcijah.
- CN− — močan nukleofil za tvorbo C–C vezi (npr. cianiranje).
- N3− (azid) — uporaben v organski sintezi in klik kemiji.
- Halogenidi (I−, Br−, Cl−) — pogosto uporabljen nukleofil pri substitucijah; relativna moč je odvisna od topila.
- HS−, RS− (tiolati) — močni in polarizabilni nukleofili, reaktivni pri napadih na karbonilne in alkilne centre.
- NH3, amini — nevtralni nukleofili, pogosto za addukte in substitucije.
Praktični nasveti
- Če želite povečati hitrost SN2 reakcije, izberite močan, malo sterično obremenjen nukleofil in aprotitično topilo.
- Za reakcije, občutljive na bazo (npr. eliminacije), uporabite manj bazične, a še vedno učinkovite nukleofile ali prilagodite topilo in temperaturo.
- Uporaba polarizabilnih nukleofilov (S-, I-) pogosto zmanjša stradanje z nadomestitvijo v protitičnih medijih.
Zaključek
Nukleofilnost je ključna lastnost v mnogih organskih in anorganskih reakcijah. Razumevanje dejavnikov, kot so naboj, elektronegativnost, velikost, sterika in topilo, omogoča predvidevanje in nadzor nad potekom reakcij, še posebej pri nukleofilnih substitucijah in solvolizah.