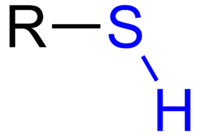
Tiol je molekula s skupino R-SH. Tioli so analogi alkoholov, kjer je kisik v hidroksilni skupini zamenjan z žveplom: z zamenjavo kisikovega atoma z žveplovim. Tioli imajo pogosto zelo močan in neprijeten vonj; zato se nekatere snovi iz skupine tiolov uporabljajo kot dodatek zemeljskemu plinu, da bi ga ljudje lahko vohali in tako odkrili puščanja. To je pomembno, ker metan sam po sebi nima vonja, vendar je lahko nevarno eksploziven.
Struktura in osnovne fizikalno-kemijske lastnosti
Tioli vsebujejo funkcionalno skupino -SH (sulfhidrilna ali tiolna skupina). V primerjavi z alkoholnimi OH-skupinami so S–H vezi običajno nekoliko daljše in šibkejše. Tioli so običajno manj polarni kot analogni alkoholi in imajo pogosto nižje vrelišče kot sorodne spojine z oksigenom iste molekulske mase.
Tioli se zelo lahko oksidirajo — najpogostejša in biološko najbolj pomembna reakcija je tvorba disulfidne vezi (R–S–S–R) iz dveh tiolov. Pri močnejši oksidaciji se lahko tvorijo tudi sulfenilne, sulfinilne ali sulfonilne kisline.
Kisline, baze in reaktivnost
Tioli so precej kisli — pKa alifatskih tiolov je običajno okoli 10–12, kar pomeni, da so precej bolj kisli kot alkoholi (pKa alkoholi ~16–18). Ko tiol odda proton in nastane tiolatni anion (R–S−), ta anion deluje kot močan nukleofil in kot reducent. Tiolni anioni so "mehkejši" nukleofili v smislu HSAB teorije, zato reagirajo raje z mehkejšimi elektrofili (npr. z alkilnimi halogenidi ali z disulfidi).
Tipične reakcije vključujejo:
- Nukleofilna substitucija (SN2) pri nastanku tioeterjev (R–S–R') z alkilacijami — povezano z nukleofilna substitucija.
- Tvorba disulfidnih vezi (R–S–S–R) z oksidacijo dveh tiolov; to je reverzibilna reakcija v bioloških sistemih.
- Adicija na elektron-privlačne dvojne vezi (Michaelova adicija) in alkilacije za označevanje ali zaščito tiolnih skupin v sintetični kemiji.
Vloga v biokemiji in biologiji
Tiolne skupine so ključne v mnogih biokemijskih procesih. Ena od naravnih aminokislin, cistein, ima v svoji strukturi tiol in je pomembna za strukturo in funkcijo beljakovin. Dve cisteinski ostanki lahko tvorita disulfidno vez, ki stabilizira terciarno ali kvartarno strukturo beljakovin. Poleg tega ima veliko encimov katalitično pomemben cisteinski ostanek (npr. cisteinske proteaze), kjer tiol sodeluje pri prenosu elektronov ali nukleofilnih reakcijah.
V celicah so tioli tudi ključni pri vzdrževanju redoks ravnovesja — najpomembnejši majhen tiol v celicah je glutation (GSH), ki ščiti pred oksidativnim stresom in sodeluje pri detoksikaciji. Procesi, kot so tiol–disulfidna izmenjava in redoks regulacija s pomočjo tiolnih skupin, so temelj mnogih celičnih mehanizmov.
Uporaba v industriji in vsakdanjem življenju
- Dodajanje kot indikatorja za izpuščanje zemeljskega plina (merkaptani), ker imajo nizko vonjalno mejo in omogočajo zgodnje zaznavanje puščanja.
- Organska sinteza: tioli in tiolati se uporabljajo za pripravo tioeterjev, kot zaščitne skupine, za sintetiko sulfidov in pri tvorbi katalitsko aktivnih centrov.
- Industrija gume: žveplene spojine in tioli sodelujejo pri procesu vulkanizacije.
- Kot ligand za kompleksiranje prehodnih kovin in v procesih odstranjevanja težkih kovin zaradi močne afinitete žvepla do kovin.
Detekcija in merjenje
Tioli so zaznavni že pri zelo nizkih koncentracijah (večina ima neprijeten vonj pri ppb do ppm ravneh). V laboratorijih in industriji se za kvantifikacijo prostih tiolov uporablja več reagenc, med njimi reagens Ellmana (DTNB), ki tvori barvni produkt z prostimi tioli. Obstajajo tudi instrumentalne metode (GC–MS, HPLC) za identifikacijo in merjenje tiolov.
Varnost
Tioli so pogosto vnetljivi in mnogi so strupeni ali vsaj neprijetni zaradi močnega vonja. Zaradi nizkih vonjalnih mej se pogosto uporabljajo kot varnostni dodatek v gorljivih plinih, vendar je pri ravnanju z njimi potrebna skrb zaradi potencialne toksičnosti in draženja dihalnih poti. Pri delu v laboratoriju priporočamo ustrezno prezračevanje, uporabo rukavic in zaščitnih očal.
Sklep
Tioli (merkaptani) so pomembna skupina žveplovih organskih spojin z značilno -SH skupino. Njihova reaktivnost — kisla narava S–H, nastanek tiolatov, močna nukleofilnost in nagnjenost k oksidaciji v disulfide — jih naredi ključne v organski kemiji, industriji in biokemiji. V biologiji omogočajo stabilizacijo beljakovinskih struktur in sodelujejo v redoks procesih, pri čemer so primeri kot cistein in glutation temeljni za celično funkcijo.