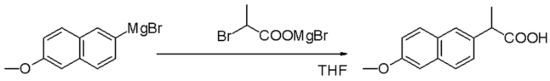
Grignardova reakcija (izgovori se /ɡriɲar/) je organokovinska kemijska reakcija, pri kateri alkil- ali aril-magnezijevi halogenidi (Grignardovi reagenti) reagirajo kot močni nukleofili in napadajo elektrofilne ogljikove atome, najpogosteje v polarnih vezah, kot je karbonilna skupina. Rezultat je tvorba nove vezi ogljik–ogljik, kar naredi Grignardovo reakcijo osnovno orodje pri sintezi organskih spojin.
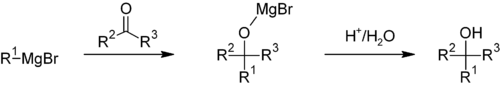
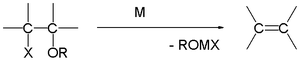
Osnovni koraki in mehanizem
Grignardov reagent se pripravi z reakcijo organskega halida (R–X) z magnezijem v eterskem topilu (npr. dietil eter ali tetrahydrofuran, THF). V praksi reagent v raztopini običajno ne obstaja kot prost karbanion, temveč kot kompleks organomagnezijevega grozda, koordiniran z molekulami etra.
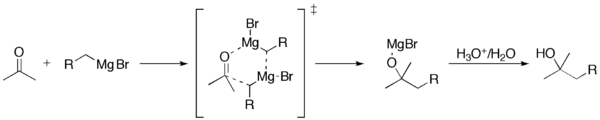
Tipičen mehanizem adicije na karbonil vključuje:
- koordinacija karbonilne kisikove lone pare na Mg, kar polarizira C=O vezi,
- nukleofilni napad ogljikovega centra reagentovega R– dela na C=O ogljik,
- nastanek alkoksidnega intermediata (Mg–O vezi),
- končna protonacija alkoksida v delovnem upoštevanem delu z dodanim protinom (npr. v vodi ali razredčeni kislini) in tvorba ustreznega alkohola ali druge produktne funkcije.
Primer: napad Grignardovega reagent R–MgX na aldehid daje sekundarni alkohol po hidroksilni protonaciji; na keton pa terciarni alkohol (če R ni vodik). Reakcija z CO2 vodi po delovanju k nastanku karboksilne kisline po kisli delni hidraciji.
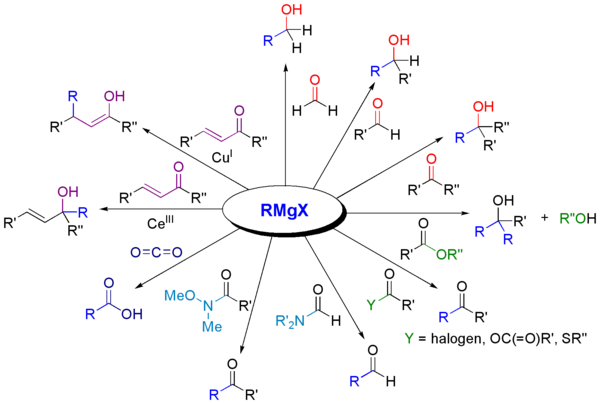
Vrste transformacij
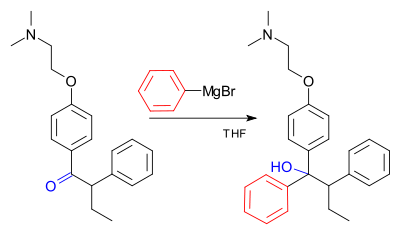
- Adicija na aldehide in ketone → primarni, sekundarni ali terciarni alkoholi (odvisno od substrata).
- Reakcija z esteri → po dveh ekvivalentih reagentov običajno terciarni alkohol (en del napada ester, drugi pa produkt acilacije).
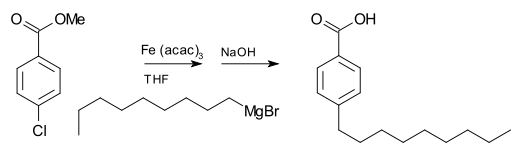
- Reakcija z karboksilnimi derivati in anorganskimi elektrofili (npr. CO2) → karboksilne kisline po obdelavi z vodo/acidom.
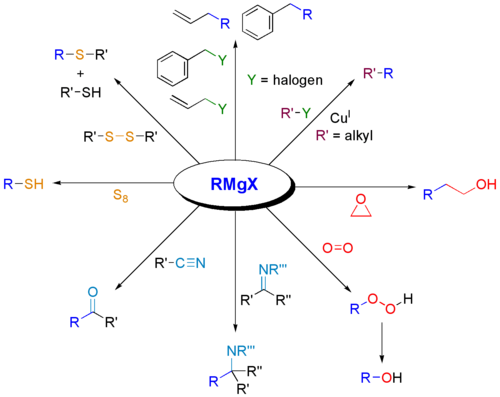
- Odpiranje epoksidov → linearni ali razvejani alkoholi (napad na manj substituirani ogljik).
- Reakcije z nitrili → po hidrolizi nastanejo ketoni.
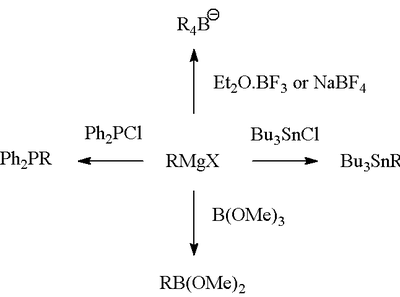
- Uporaba pri metalo-organskih pretvorbah (npr. tvorba vezi ogljik–bor, ogljik–fosfor) pri nadaljnjih stopnjah sinteze.
Lastnosti in omejitve
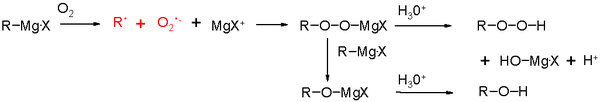
Grignardovi reagenti so zelo močni nukleofili in tudi močni baze. Ker imajo konjugirane kisline (R–H) zelo visoke vrednosti pKa (približno 50 za enostavne alifatske vodike), je karbanionska narava R− zelo basa: reagenti zlahka odstranjujejo protone iz snovi, ki imajo kisle protone. Zato so Grignardovi reagenti izjemno občutljivi na prisotnost vode, alkoholov, aminov, karboksilnih kislin in drugih funkcionalnih skupin, ki vsebujejo kisle protone — ti reagenti jih hitro protonirajo in deaktivirajo (sprememba izkoristka).
Praktične posledice:
- Stroga suhost in inertna atmosfera: reakcije se običajno izvajajo v suhi posodi pod argonom ali dušikom.
- Topila: uporabljajo se etrska topila (dietil eter, THF), ki koordinirajo Mg in stabilizirajo reagent.
- Aktivacija magnezija: površina magnezija je pogosto pasivirana; sprejmejo se metode, kot so ogrevanje plamena, dodatek joda ali ultrazvok, da se aktivira površina in zmanjša občutljivost na vlago.
Grignardovi reagenti niso enostavni ionski raztopinski karbanioni v klasičnem smislu; v raztopini predstavljajo agregate in komplekse (Schlenkova ekvivalenca: 2 RMgX ⇄ R2Mg + MgX2), zato njihovo vedenje vključuje elemente koordinacijske kemije in delno kovinsko povezanost.
Omejitve glede reakcij z alkil halidi
Obstaja specifična omejitev: Grignardovi reagenti pogosto ne reagirajo direktno z alkil halidi v standardnem SN2 mehanizmu, kot bi pričakovali od nekaterih drugih nukleofilov. Namesto tega se lahko pojavijo stranski procesi, kot so enelektronski prenosi, tvorba radikalov in kopičenje (Wurtzovo spajanje) ali razgradnja reagentov, kar pogosto vodi v nizke izkoristke. Zato je neposredna tvorba nove vezi C–C med dvema alkilom preko kombinacije Grignard + alkil halid običajno nepraktična.
Praktični nasveti in varnost
- Uporabljajte suho steklo in inertno atmosfero (N2 ali Ar).
- Preprečite prisotnost kislih funkcionalnih skupin v reakcijski zmesi.
- Pri začetni pripravi reagenta je pogosto potrebno aktivirati magnezij (čiščenje površine, dodatek joda ali ultrazvoka).
- Grignardovi reagenti so reaktivni in včasih vnetljivi — ravnajte z njimi previdno in upoštevajte laboratorijske varnostne postopke.
Zgodovina
Reakcijo in reagente je odkril François Auguste Victor Grignard. Po njem so poimenovani Grignardovi reagenti; za svoje delo je prejel Nobelovo nagrado za kemijo leta 1912 (Univerza v Nancyju, Francija).
Povzetek: Grignardova reakcija je vsestransko in močno orodje za tvorbo vezi ogljik–ogljik in drugih funkcionalnosti v organski sintezi, a zahteva suhe razmere, primerno topilo in previdnost pri izbiri substratov zaradi občutljivosti reagenta na vodne in kisle skupine.