Reakcija SN 2 (znana tudi kot dvomolekularna nukleofilna substitucija) je substitucijska reakcija v organski kemiji. Gre za vrsto nukleofilne substitucije, pri kateri osamljeni par nukleofila napade elektronsko pomanjkljiv elektrofilni center in se nanj veže. Pri tem se izloči druga skupina, imenovana "odhajajoča skupina". Tako prihajajoča skupina v enem koraku nadomesti odhajajočo skupino. Ker sta v počasnem koraku reakcije, ki določa hitrost, vključeni dve reagirajoči vrsti, je to pripeljalo do imena dvomolekularna nukleofilna substitucija ali SN 2. Med anorganskimi kemiki je reakcija SN 2 pogosto znana kot mehanizem izmenjave.
Mehanizem
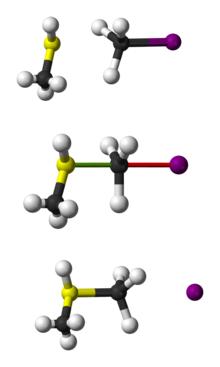
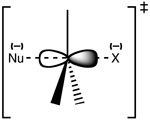
Reakcija SN 2 poteka v enem concerted (sočasnem) koraku brez preprostih intermediata z ločenim nabojem. Nukleofil napade elektrofilni ogljikov atom z nasprotne strani glede na odhajajočo skupino (t. i. "backside attack"), pri čemer se oblikujeta delna vez med nukleofilom in ogljikom ter postopno oslabi vez med ogljikom in odhajajočo skupino. V maksimumu energije (prehodno stanje) je ogljik delno pentakoordiniran, vezni deli so delno ustvarjeni in delno razgrajeni, nato pa se odhajajoča skupina loči in nova vez se dokončno oblikuje.
Kinetika
Hitrost SN 2 reakcije je odvisna od koncentracij obeh reaktantov in sledi zakonitosti drugega reda:
- Hitrost: v = k [nukleofil] [substrat–LG]
- Ker v počasnem koraku sodelujeta dve snovi, je reakcija dvomolekularna glede na hitrost določajoči korak.
Stereokemija
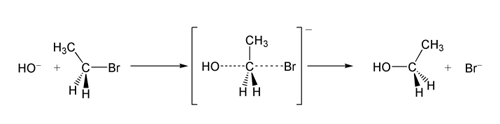
Posledica zadnjega napada z nasprotne strani je inverzija konfiguracije na stereocentru (Waldenova inverzija). Če je izhodišče enantiomer, bo produkt nasprotno konfiguriran; to je pomembno pri sintezi kiralnih spojin in v organski sintezi, kjer se stereokemija prenaša neposredno skozi mehanizem SN 2.
Dejavniki, ki vplivajo na hitrost
- Struktura substrata: Manj sterično oviran ogljik pospešuje SN 2. Hitrost običajno pada v vrsti: metil > primaren > sekundaren >> terciaren (terciarni substrati skoraj ne reagirajo po SN 2 zaradi steričnega oviranja).
- Nukleofil: Močni, nabiti nukleofili reagirajo hitreje kot šibkejši. Osnovnost je pogosto korelirana z reaktivnostjo, vendar polarizabilnost in topilo lahko spremenita trend.
- Odhajajoča skupina: Bolj stabilen anion (boljša odhajajoča skupina) pospešuje reakcijo. Na primer, iodid je običajno boljši od bromida, ki je boljši od klorida.
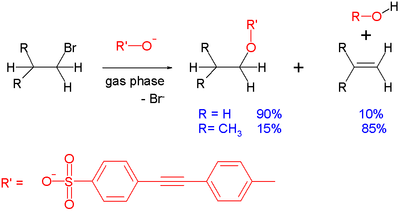
- Topilo: Polarno aprotična topila (npr. acetont r, DMF, DMSO) pospešijo SN 2, ker ne solvatizirajo močno nukleofilov; polarna proticna topila (npr. voda, alkohol) lahko zavirajo reakcijo zaradi močne solvatacije nukleofilov.
- Temperatura in koncentracije: Višja temperatura običajno poveča hitrost; višje koncentracije reaktantov tudi povečajo hitrost glede na kinetični zakon.
Primeri
- Methanolizacija metilklorida z hidroksidom: CH3Cl + OH− → CH3OH + Cl− (koncerted napad OH− na metilni ogljik).
- Substitucije pri primarnih alkilhalogenidih: n-prililbrm + CN− → n-prilil-cianid + Br− (SN 2 pot poteka z visokim izidom pri močnih nukleofilih v polarno aprotičnih topilih).
Primerjava s SN 1
- SN 2 je concerted in dvomolekularen (hitrost odvisna od dveh vrst), medtem ko SN 1 poteka preko karbokationa kot intermediata in je enomolekularen v hitrostno določujočem koraku (hitrost odvisna samo od substrata).
- Sterični vpliv in topilo pogosto določata, ali bo substrat sledil SN 1 ali SN 2 poti (na primer terciarni substrati in polarna proticna topila podpirajo SN 1; metilni in primerni substrati v polarno aprotičnih topilih pogosteje sledijo SN 2).
Praktične napotke
- Za izvedbo SN 2 reakcij izberite močan nukleofil in polarno aprotično topilo, kadar želite pospešiti substitucijo.
- Izogibajte se steričnim oviram na elektronskem centru, če želite visok izkoristek SN 2 nad SN 1.
Sklep: SN 2 je temeljni mehanizem v organski kemiji, ključen za razumevanje, kako se vezi lomijo in tvorijo med substitucijami, z značilno concerted mehaniko, zakonitostjo hitrosti drugega reda in Waldenovo inverzijo stereokemije.