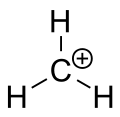
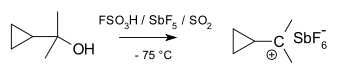
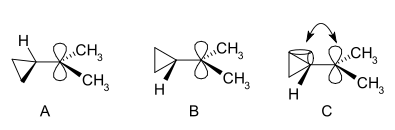
Karbokation je ion s pozitivno nabitim ogljikovim atomom. Nabiti ogljikov atom v karbokationu ima le šest elektronov v zunanji valenčni lupini (to pomeni, da ima "sekstet" namesto običajnega okteta), torej v njej manjkajo dva elektrona, ki bi zapolnila elektronov do osmih. Ogljik s popolnim oktetom je termodinamsko najbolj stabilen (pravilo okteta), zato so karbokationi običajno reaktivni in se trudijo zapolniti oktet ter ponovno pridobiti nevtralen naboj.
Struktura in hibridizacija
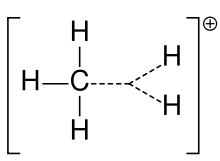
Na prvi pogled bi karbokation razumeli kot ogljik s sp3 hibridizacijo z eno prazno sp3 orbitalo, kar bi dalo tetraedrsko geometrijo. V praksi pa je elektronika takih centrov bližje sp2 hibridizaciji: karbokation ima prazno p-orbitalo pravokotno na ploskev treh vezav in posledično približno trigonalno planarno geometrijo. Ta konfiguracija omogoča delokalizacijo pozitivnega naboja preko p-orbitale in pojasni opazno stabilizacijo pri določenih substituentih.
Vrste karbokationov
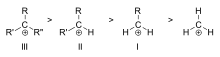
- Primarni, sekundarni, tercierni — glede na število ogljikov, vezanih na nabiti center. Tercierni karbokationi so običajno najbolj stabilni zaradi večje možnosti hyperkonjugacije in induktivne stabilizacije.
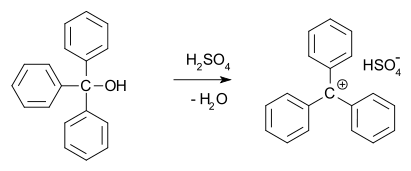
- Alilni in benzilni — karbokationi, kjer je nabiti center povezan z dvojno vezjo ali aromatskim sistemom; takšni centri se stabilizirajo z rezonanco.
- Vinilni in arilni — karbokationi, kjer je nabit karbon del dvojne vezi ali aromatičnega obroča; ti so praviloma zelo nestabilni, ker p-orbitala ne more enostavno delokalizirati naboja.
Faktorji stabilnosti
- Induktivni učinek: alkilne skupine s pozitivnim polarizacijskim učinkom preusmerijo gostoto proti nabitemu centru in ga stabilizirajo.
- Hyperkonjugacija: delokalizacija naboja preko σ-veze C–H ali C–C, ki je izrazito pri sekundarnih in terciernih karbokationih.
- Resonančna stabilizacija: če lahko pozitiven naboj delokaliziramo na sosedeče π-sisteme (npr. alilni, benzilni karbokation), je stabilnost pomembno povečana.
- Solventni in ionski učinki: polarna topila in soli (npr. superkislini) lahko stabilizirajo karbokation preko solvatacije in ionnih parov.
- Sterični učinki: močne sterilne motnje lahko v nekaterih primerih ovirajo stabilizacijo, a včasih dodatne alkilne skupine še vedno povečajo stabilnost zaradi hyperkonjugacije.
Nastanek karbokationov in mehanizmi
Karbokationi nastanejo v različnih organskih reakcijah, najpogostejši poti so:
- Heterolitična cepitev C–X (kjer X = halogen, OH po protonaciji): odcep več elektronov na enega partnerja pušča pozitiven naboj na ogljiku.
- Protonacija alkenov v kislih medijih, ki vodi do nastanka karbokationa (Markovnikovova adicija).
- Ionizacija estrov, etrov ali drugih funkcionalnih skupin v močno kislih pogojih.
- Redukcijsko-oksidacijski in fotokemični procesi, kjer se sproži heterolitična razpoka vezi.
Reaktivnost in lastnosti
- Nukleofilni napadi: karbokation je elektrofilen center; najbolj običajna reakcija je hitra vezava nukleofila, ki zapolni oktet in tvori novo vez.
- Eliminacije: karbokationi so med intermediati v E1 mehanizmih, kjer vodijo do nastanka alkenov.
- Rearanžmaji (hidridni ali alkilni preskoki): karbokationi pogosto prehajajo v bolj stabilne strukture z migracijo skupin (npr. hidridni premik iz sosednjega ogljika), kar vpliva na produkt reakcije.
- Hammondovo načelo pomaga napovedati, ali bo intermediat bolj “reaktiven” ali “stabilen” glede na energijo prehodnega stanja in naravo reakcije.
Opazovanje in uveljavljenost pojma
Karbokationi so pogosto kratkotrajni intermediatni tipi, a jih je možno opazovati ali stabilizirati v posebnih pogojih:
- Spektroskopske metode (NMR pri nizkih temperaturah, IR, UV–Vis) in lovilci nukleofilov omogočajo zaznavo ali zajetje karbokationov.
- Razvite so zelo stabilne, isolirane karbokationske soli (npr. s perfluoriranimi anioni), ki omogočajo neposredne študije strukture.
- V zgodovini sta bila izraza carbenium in carbonium uporabljena za različne tipe pozitivnih ogljikovih ionov; danes se za običajne trivalente pozitivne ogljikove centre uporablja izraz karbokation.
Pomembni koncepti za organske reakcije
- Pri načrtovanju reakcij je ocena relativne stabilnosti karbokationov ključna za napoved produktov (npr. ali bo prišlo do rearranžmaja).
- Razumevanje vpliva substituentov in topila omogoča nadzor nad selektivnostjo (kinetska vs. termodinamska kontrola).
- Karbokationi igrajo osrednjo vlogo v mnogih industrijskih procesih in laboratorijskih transformacijah, kot so alkilacije, izomerizacije in polimerizacije.
Sklep: Karbokationi so klasični elektrofili z značilno prazno p-orbitalo in približno trigonalno planarno geometrijo. Njihova stabilnost in reaktivnost sta odvisni od substitucije, resonance, hyperkonjugacije in okolijskih pogojev — razumevanje teh dejavnikov je temelj pri napovedovanju poteka številnih organskih reakcij.