Reakcija NS1 je substitucijska reakcija v organski kemiji. Izraz "SN" pomeni nukleofilno substitucijo, številka "1" pa označuje, da je v hitrostno določujočo fazo vključena samo ena molekula reagenta (unimolekularna). Reakcija poteka preko vmesnega produkta, karbokationa, in jo pogosto imenujejo tudi dissociativni mehanizem. Prvi predlog tega reakcijskega mehanizma sega v delo Christopherja Ingolda in sodelavcev v 40. letih 20. stoletja.
Mehanizem
Tipični dvofazni mehanizem SN1 vključuje:
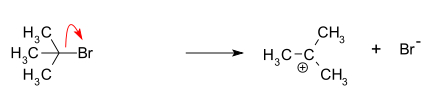
- 1. korak (hitrostno določujoč): odvzem odstopne skupine (npr. halogenida, tosilata) iz substrata in tvorba karbokationa. Ta korak je unimolekularen in najpogosteje zahteva preseganje večje energetske ovire.
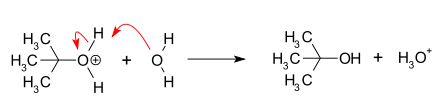
- 2. korak: nukleofil napade nastali karbokation in nastane produkt substitucije.
Ker je prvi korak hitrostno določujoč, je hitrost reakcije odvisna le od koncentracije substrata (npr. alkilnega halogenida), ne pa neposredno od koncentracije nukleofila.
Faktorski vplivi
- Struktura substrata: terciarni > sekundarni >> primarni. Terciarni alkilni halogenidi stabilizirajo karbokation z vplivom hiperkonjugacije in induktivnimi učinki.
- Odstopna skupina: dobra odstopna skupina (npr. I−, Br−, tosilat) olajša nastanek karbokationa in pospeši SN1.
- Topilo: polarna proticna topila (npr. voda, alkoholi) stabilizirajo karbokation in odstopno skupino z raztapljanjem, zato pospešijo SN1. Polarno aprotična topila pogosto podpirajo SN2 poti namesto SN1.
- Nukleofil: šibkejši nukleofili so običajno dovolj, saj napad ni v hitrostno določujočem koraku; močan nukleofil lahko spodbuja konkurenčno SN2 pot.
- Temperatura in baza: višja temperatura ter močne baze lahko povečajo delež E1 eliminacije, ki tekmuje s SN1.
Kinetika in stereokemija
Kinetika: hitrost reakcije SN1 opisuje enačba v = k [substrat] (prvi red). Eksperimentalna neodvisnost hitrosti od koncentracije nukleofila je značilni dokaz mehanizma SN1.
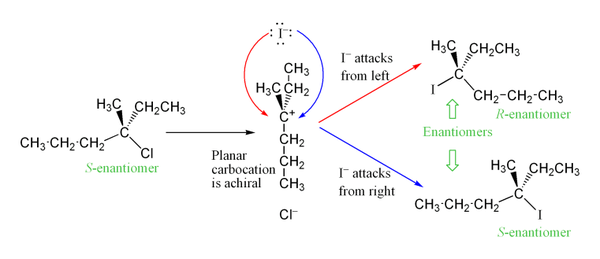
Stereokemija: ker karbokation velja za planarno (sp2) vrsto, napad nukleofila lahko poteka z obeh strani, kar pogosto vodi do racemizacije pri prezgodnjih stereoizomerih (npr. iz enantiomernega sekundarnega substrata). V praksi pa se lahko pojavijo delne ohranitev ali inverzija konfiguracije zaradi ionnih parov (intimni ali topološko vezani ion pari), kjer je dostop z ene strani omejen.
Zapleti in premiki
Vmesni karbokationi so nagnjeni k rearanžmajem (npr. hidridni prehod ali alkilni premik) v smer stabilnejšega karbokationa. Ti premiki lahko vodijo do nebolečnih produktov, ki se razlikujejo od neposredne substitucije pričakovanega mesta.
Primeri
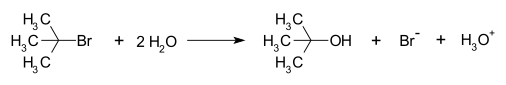
- Solvoliza tert-butil klorida v vodi: (CH3)3C-Cl + H2O → (CH3)3C-OH + HCl. Ta reakcija poteka po SN1 mehanizmu z značilnim prvo-reden kinetičnim zakonom.
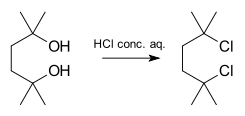
- Protonacija sekundarnih ali terciarnih alkoholov v močno kislih pogojih pogosto vodi do odstopa vode in tvorbe karbokationa, ki ga nato napade nukleofil (npr. solvoliza alkohola).
- Reakcije sekundarnih ali terciarnih alkilnih halogenidov v polarnih proticnih topilih z blagimi nukleofili običajno potekajo po SN1 poti; pri primarnih substratih je bolj verjetna alternativa SN2 (SN2).
Kako prepoznamo SN1 v praksi
- Merjenje hitrosti reakcije: hitrost neodvisna od koncentracije nukleofila (prvi red glede na substrat).
- Opazovanje racemizacije stereocentrov v produktu.
- Učinki topila: pospešitev v polarnih proticnih topilih.
- Prisotnost rearanžmov ali strukturnih produktov, ki kažejo na tvorbo karbokationa.
Če povzamemo: SN1 je unimolekularna nukleofilna substitucija, pri kateri je ključni korak disociacija substrata v karbokation in odstopno skupino. Najpogosteje jo opazimo pri terciarnih (in nekaterih sekundarnih) substratih v polarnih proticnih topilih z dobrimi odstopnimi skupinami; konkurenca s SN2 in E1 pa je odvisna od strukture, pogojev in narave nukleofila.