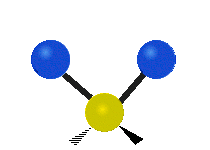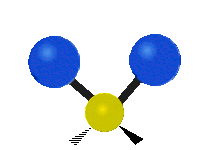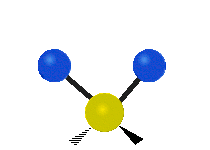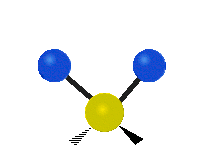
Molekulske vibracije so ena od treh osnovnih vrst gibanja molekul, poleg translacijskega gibanja (ko se celotna molekula premika v prostoru) in rotacijskega gibanja (ko se molekula vrti okoli osi). Vibracijsko gibanje opisuje premike vezi in relativne položaje atomov v molekuli — atome si lahko predstavljamo kot kroglice, povezane z vzmetmi, ki se lahko raztezajo in krčijo. Najpreprostejši primer je raztezanje vezi med dvema atomoma, kot pri diatomskih molekulah: vodik H2, dušik N2 in kisik O2.
Kaj so normalne mode in kvantizacija energije
Vsaka molekula ima določeno število neodvisnih vibracijskih vzorcev, imenovanih normalne mode. V klasičnem pogledu so to kolektivni premiki atomov, pri katerih vsi atomi nihajo s isto frekvenco. V kvantni mehaniki so te vibracije kvantizirane: energija vibracij je diskretna in je za harmonski oscilator dana z izrazom E = (n + 1/2) hν, kjer je n kvantno število, h Planckova konstanta in ν frekvenca vibracije. Frekvenco približno določimo z vzmetno konstanto vezi k in reducirano maso μ dveh sodelujočih atomov: ν ≈ (1/2π) √(k/μ). Zaradi kvantizacije obstaja tudi ničelna energija (zero-point energy), torej molekula ni povsem mirovala tudi v osnovnem stanju.
Koliko vibracij ima molekula?
Število normalnih modov je odvisno od števila atomov N v molekuli in njene geometrije:
- nelinearna molekula: 3N − 6 vibracijskih načinov;
- linearna molekula: 3N − 5 vibracijskih načinov (ena rotacijska stopnja svobode manj).
Vrste vibracij
Običajno ločimo osnovne tipe vibracij, ki se pojavljajo kot normalne mode:
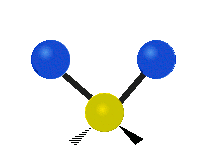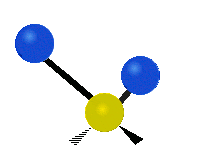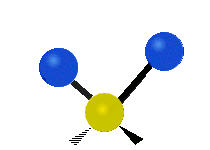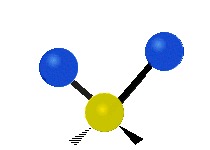
- Raztezanje (stretching) — sprememba razdalje med dvema atomoma. Lahko je simetrično (več vezi se razteza in krči istočasno) ali asimetrično (ene vezi se raztezajo, druge krčijo).
- Upogibanje (bending) — sprememba kota med vezmi. Podvrste so scissoring (škarjasta), rocking (gugalna), wagging (mahanje) in twisting (zavijanje).
- Izvenplaščinske (out-of-plane) vibracije — atomi se premikajo iz ravnine molekule.
- Torzijone (torsional) — rotacija okoli vezne osi (pomembno pri velikih organskih molekulah).
Spektroskopija: kako merimo vibracije
Vibracije so osnova infrardeče (IR) in Ramanove spektroskopije. Pri IR-spektroskopiji absorbcija elektromagnetnega valovanja povzroči prehod v višje vibracijsko stanje, vendar je pogoj za IR-aktivnost sprememba dipolnega momenta med vibracijo. Ramanova spektroskopija zaznava spremembe v polarizabilnosti molekule in zato pogosto dopolnjuje IR. Za idealen harmonski oscilator je pravilo za prehode Δv = ±1, vendar anhamoničnost omogoča tudi overtone (Δv = ±2, ±3 …) in kombinirane pasove.
Primeri vibracij v znanih molekulah
- Diatomske molekule (vodik H2, dušik N2, kisik O2) imajo samo en vibracijski način — raztezanje/krčenje vezi.
- CO2 (linearna): ima simetrično raztezanje (IR-inaktivno, Raman-aktivno), asimetrično raztezanje (IR-aktivno) in dva enaka upogibna načina (degenerirana).
- H2O (nelinearna): tri vibracijske mode — simetrično in asimetrično raztezanje ter upogibanje (bending); vse so IR-aktivne zaradi spremembe dipolnega momenta.
- CH skupine in organski funkcionalni skupini: C–H, O–H in N–H vezi dajejo značilne pasove v IR spektru; torzijske in upogibne mode pogosto določajo obliko večjih molekul.
Zakaj so molekulske vibracije pomembne?
Razumevanje vibracij je ključno za interpretacijo spektrov, določanje strukture molekul, preučevanje kemijskih vezi in reakcijskih poti ter za aplikacije v materialih, biokemiji in analitični kemiji. Vibracijske značilnosti nam povedo o jakosti vezi, masi atomov in simetriji molekule, zato so nepogrešljivo orodje v raziskavah in industriji.
Za dodatno poglobitev lahko raziščete pojme, kot so vibracije v kvantni mehaniki, normalni načini ter eksperimentalne metode za njihovo merjenje.