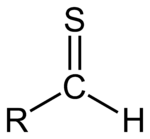
Definicija in struktura
Tial ali tioaldehid je vsaka molekula s funkcionalno skupino RC(S)H. Gre za analog aldehida, pri katerem je kisik v ogljikovi karbonilni skupini (=C=O) zamenjan z žveplom, tako da nastane skupina C=S z vezjo C–S. Žveplo nosi dve osamljeni para elektronov in sodeluje v dvojni vezi z ogljikom. Zaradi večje atomske velikosti in boljše polarizabilnosti žvepla se lastnosti C=S razlikujejo od običajne C=O vezi.
Reaktivnost in stabilnost
Tiali so običajno zelo reaktivni. Ker je ogljikov atom v C=S močan elektrofil, hitro reagira z nukleofili ali pa z drugimi molekulami iste vrste. V praksi se tiali pogosto ne izolirajo, ker takoj, ko nastanejo, reagirajo sami s seboj ali z okoliškimi reagent(i) in tvorijo dimerje, polimere ali ciklične produkte.
Ena izmed pogostih procesnih poti so Diels-Alderjeve reakcije in druge periciklične reakcije, kjer tioaldehidi delujejo kot zelo aktivni dienofili. Zaradi te reaktivnosti se v sintetični kemiji tioaldehide običajno generira in uporabi in situ (tj. v prisotnosti drugega reagenta, ki takoj ujame produkt).
Stabilnost tioaldehidov se poveča z uvedbo velikih (sterično zahtevnih) substituentov R, ki preprečijo medmolekulske interakcije in dimerizacijo. V nekaterih primerih stabilizirajo tudi konjugacija z aromatskim obročem ali atomske skupine, ki razpršijo pozitivno naboj na ogljikovem centru.
Razlika med tiali in tioketoni
Če je atom vodika v skupini RC(S)H zamenjan z drugo organsko R-skupino, dobimo tioketon (RRC(S)). Tioketoni so na splošno stabilnejši od tioaldehidov, saj jim manjša reaktivnost aldehidnega vodikovega centra in večja substitucijska zaščita preprečujeta hitro samoreakcijo. Mnogo znanih in uporabnih tioketonov (npr. arilni tioketoni) je izoliranih in uporabljanih v organični sintezi.
Priprava in praktična uporaba
- V laboratorijih se tioaldehidi pogosto pridobivajo z thionacijo običajnih aldehidov z reagent(i), kot so Lawessonov reagent ali P4S10, vendar je neposredna priprava tioaldehidov redka zaradi njihove kratke življenske dobe.
- Pogoste strategije vključujejo tvorbo tioaldehida in situ in takojšnje zajetje v ciklične produkte (npr. v Diels–Alderjevih ali [2+2] cikloadicijah) ali reakcije z nukleofili.
- Nekateri stabilni tioketoni, kot je na primer tiobenzofenon (diphenylthioketone), se uporabljajo kot reagent(i) ali modelni spojini pri preučevanju reaktivnosti C=S vezi.
Spektroskopske značilnosti
Tioaldehidi in drugi tiokarbonili imajo prepoznavne spektroskopske lastnosti: v IR-spektru se zazna absorpcija zaradi C=S vezi pri nižjih valovnih številih kot običajna C=O absorpcija (območje se lahko razlikuje glede na substitucijo). V 1H-NMR je signal za C–H (aldehidni proton) običajno v območju, značilnem za aldehidne protone, vendar lahko zaradi bližine žvepla pride do sprememb kemijskega premika. Ker so ti spojini pogosto zelo reaktivni, jih je v spektroskopskih meritvah pogosto mogoče zaznati le pri zelo nizkih temperaturah ali v matričnih pogojih.
Povzetek
- Tial (tioaldehid) je spojina s skupino RC(S)H — aldehid, kjer je O zamenjan z S.
- So močni elektrofilni centri in zato zelo reaktivni; pogosto reagirajo sami s seboj (dimerizacija, polimerizacija) ali sodelujejo v pericikličnih reakcijah, npr. Diels-Alderjevih.
- Stabilnost se poveča z velikimi steričnimi substituenti ali zogenimi stabilizacijskimi učinki; tioketoni (RRC(S)) so na splošno bolj stabilni od tioaldehidov.
- V praksi jih pogosto generiramo in uporabimo in situ, pri nizkih temperaturah ali v prisotnosti partnerjev, ki jih takoj ujamejo.