Obstaja več alotropov ogljika. Najbolj znana sta diamant in grafit. Grafit je prevodnik, polkovina (element, ki je delno kovina in nekovina, na primer črni fosfor in sivi selen). Uporablja se lahko na primer kot material v elektrodah električnih obločnih svetilk. Grafit je najbolj stabilna oblika trdnega ogljika, kar so jih kdaj koli odkrili.
Alotropi so različne oblike istega kemijskega elementa. Vsi elementi so sestavljeni iz lastnih atomov. Vse fizikalne razlike so posledica načina združevanja atomov. Številni elementi so alotropni, ker je mogoče atome med seboj povezati na več načinov. Prav tako obstajajo različni načini, kako se lahko molekule razporedijo v večje strukture.
Diamant je eden najbolj znanih alotropov ogljika. Zaradi svoje trdote in visoke razpršitve svetlobe je primeren za uporabo v nakitu. Uporablja se tudi v industriji. Diamant je najtrši znani naravni mineral. Zaradi tega je odličen abraziv. Diamant tudi dobro ohranja svoj sijaj. Tako diamant kot grafit imata izredno visoko tališče, kar je nenavadno za nekovinski element.
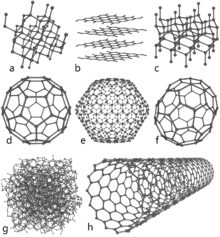
Osnovne vrste alotropov ogljika
- Grafit – slojevita struktura z vezmi sp2; sloji so med seboj šibko povezani, zato se grafit lomi po plasteh. Dober električni prevodnik v ravnini slojev, uporaben kot mazivo, material za svinčnike, elektrode in visokotemperaturne komponente.
- Diamant – tridimenzionalna mreža z vezmi sp3, kjer je vsak atom ogljika vezan na štiri druge v tetraedrični geometriji. Izjemno trd, z visoko toplotno prevodnostjo in veliko optično razpršitvijo; rabi v nakitu in kot industrijsko orodje (rezila, svedri, brusni materiali).
- Grafen – enoslojna, enojna ploskev ogljikovih atomov v šesterokotni mreži; iz njega izhajajo številne izjemne lastnosti: zelo visoka električna in toplotna prevodnost, velika mehanska trdnost in fleksibilnost. Osnova za razvoj nanoelektronike in senzorjev.
- Fulereni (npr. C60) – molekule v obliki votlih kroglic (»buckyballs«); zanimivi za raziskave v materialih, medicini in kot nosilci zdravil.
- Ogljikove nanocevke – valjaste strukture, sestavljene iz zavitih grafenskih listov; lahko so kovinske ali polprevodniške glede na zavitje (chirality). Uporabne za ojačanje materialov, v elektroniki in kot vodniki toka na nanometerski ravni.
- Amorfni ogljik – brez dolgoročnega urejenega kristalnega reda (npr. premog, aktivno oglje, katranske oblike). Raznolike lastnosti odvisno od vsebnosti sp2/sp3 vezi; uporabno kot filtrirni material, absorbent in polnilo.
- Lonsdaleit – redka naravna oblika (pretežno v meteoritih), struktura podobna diamantu a s heksagonalno kristalno mrežo; teoretično zelo trda.
Zakaj se lastnosti tako razlikujejo?
Razlike med alotropi izhajajo iz vrste vezi (sp2 proti sp3), razporeditve atomov in dimensionalnosti strukture. Na primer:
- V diamantu sp3 vezi tvorijo trdno tridimenzionalno mrežo — posledica je ekstremna trdota in visok toplotni prevod.
- V grafitu sp2 vezi tvorijo močne ploskve, med katerimi delujejo šibke van der Waalsove sile — zato je grafit mehkejši in se lomi po plastih ter dobro prevaja elektriko v ravnini slojev.
- Grafen in nanocevke izkoriščajo elektron delokalizacijo v sp2 mreži, kar daje izjemne električne in mehanske lastnosti.
Lastnosti — povzetek
- Trdota: diamant ≈ najtrši znani naravni mineral (Mohsova lestvica 10).
- Električna prevodnost: grafit in grafen sta dobri prevodnici; diamant je izolator (lahko pa pri dopingih prevaja).
- Toplotna prevodnost: diamant ima izjemno visoko toplotno prevodnost; grafen in nanocevke tudi izstopajo v tem pogledu.
- Optične lastnosti: diamant močno lomi svetlobo, kar daje značilen sijaj; grafit je temen in mat.
- Tališče: oba (diamant in grafit) imata zelo visoko tališče za nekovinski element, kar je posledica močnih kovalentnih vezi.
Nastanek in proizvodnja
Nekateri alotropi nastajajo naravno (diamanti v zemeljski kori, grafit v metamorfnem kamninju, fulereni v atmosferskih razmerah z močnim segrevanjem). Poleg tega so ključne tudi umetne metode:
- HPHT (High Pressure High Temperature) – sintetiziranje diamantov pod visokim tlakom in temperaturo, posnemajo naravne razmere.
- CVD (Chemical Vapor Deposition) – kemična usedlina iz plina, omogoča rast tankih diamantnih plasti ali grafena na podlagi.
- Izdelava grafena z luščenjem (»scotch tape« metoda), kemičnim usedanjem ali epitaksialno rastjo na podlagah.
- Polimerizacija in kondenzacija za tvorbo fulerenov in nanocevk v laboratorijih ter industriji.
Uporabe
- Diamant: nakit, rezila, brusni instrumenti, orodja za vrtanje, optični in toplotni prevodni elementi v elektroniki.
- Grafit: elektrode, maziva, svinčniki, termične zaščite, materiali za jedrske reaktorje (moderatorji/pravokotne strukture), komponente v visokotemperaturnih pečeh.
- Grafen in nanocevke: prihodnost v elektroniki, fleksibilnih zaslonih, visokokakovostnih kompozitih, baterijah, superkapacitorjih in senzorjih.
- Fulereni: raziskave v zdravilih, kot molekularni nosilci in v materialih z zanimivimi elektronskimi lastnostmi.
- Amorfni ogljik: filtracija, čiščenje, adsorpcija, pigmenti in polnila.
Kratki povzetek
Alotropi ogljika pokažejo, kako ista vrsta atomov lahko ob različnih povezavah in razporeditvah tvori materiale z zelo različnimi lastnostmi — od najtršega minerala (diamant) do mehko plastnega prevodnika (grafit) in do naprednih nanomaterialov (grafen, nanocevke, fulereni). Razumevanje teh struktur omogoča razvoj novih tehnologij in izboljšanje obstoječih industrijskih procesov.