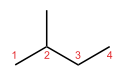Strukturni izomerizem (IUPAC ga imenuje konstitucijski izomerizem) je vrsta izomerizma. Dve kemikaliji v tej izomeriji imata enako molekulsko formulo, vendar sta se molekuli povezali v različnih zaporedjih. Nasprotje strukturni izomeriji je stereoizomerija: pri strukturnih izomerih se razlikuje način vezave atomov (povezave), pri stereoizomerih pa je razlika v tridimenzionalni razporeditvi istih povezav. Strukturni izomeri zato pogosto pokažejo različne fizikalne in kemične lastnosti, na primer vrelišče, vreliščno maso, topnost in reaktivnost.
Vrste konstitucijskega (strukturnega) izomerizma
- Skeletni (verižni) izomeri: razlikujejo se v zgradbi ogljikovega ogrodja (razvejanost verige). Primer: C4H10 — n-bután (nevejan) in izobután (razvejan) sta skeletna izomera.
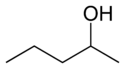
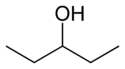
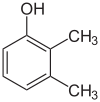
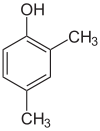
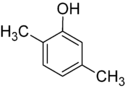
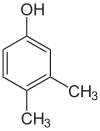
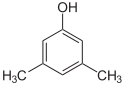
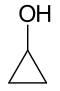
- Položajni (pozicijski ali regio) izomeri: imajo enako ogrodje in funkcionalne skupine, a se funkcionalne skupine ali vezi nahajajo na različnih mestih v molekuli. Primer: 1-propanol in 2-propanol (oba C3H8O) se razlikujeta po položaju -OH skupine.
- Funkcijski izomeri: imata iste atomske sestave, vendar različne funkcionalne skupine, kar vodi do popolnoma različnih kemijskih lastnosti. Primer: etanol (alkohol) in dietil eter (eter) ali tudi etanol in dimetil eter (oba C2H6O).
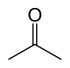
- Tautomeri: posebna vrsta funkcionalnih izomerov, ki se med seboj hitro pretvarjajo s selitvijo protona in premikom dvojnih vezi; pogosto gre za ravnotežje (npr. keto–enol). Primer: keto in enol oblika pri acetoctni kislini ali aceton–enolni tautomeri.
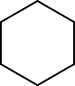
- Krožnokverižni (ring–chain) izomeri: enaka molekulska formula, različna so, če je ogrodje v krogu ali v odprti verigi. Primer: ciklopentán in penten (nekateri izomeri) imajo isto sestavo, a različne strukture.
- Metameri (manj pogosti): pojavljajo se pri spojinah z dvojnim valentnim heteroatomom (npr. etri, ketoni, amini), kjer sta alkilna dela različna, npr. R–O–R' in R''–O–R''', s skupno formulo, a različnima alkilnima skupinama.
Kako ločimo konstitucijske izomerje
Konstitucijske izomerje običajno ločimo z analitičnimi metodami:
- NMR spektroskopija (1H, 13C) pokaže razliko v okolju atomov vodika in ogljika.
- IR spektroskopija razkriva prisotnost različnih funkcionalnih skupin (npr. OH, C=O).
- Masna spektrometrija (MS) pomaga pri določanju molekulske mase in fragmentacije, ki je odvisna od strukture.
- Chromatografske tehnike (GC, HPLC) ločijo izomere glede na fizikalne lastnosti.
Pomen in posledice
Konstitucijski izomerizem je pomemben v sintetični in organski kemiji, kemijski industriji in farmaciji, ker različni izomeri z enako formulo pogosto kažejo zelo različne lastnosti, varnostne profile in bioločno aktivnost. Poznavanje vrst izomerizma pomaga pri načrtovanju sintez, analiz in pri pravilnem prepoznavanju snovi v raziskavah ter v industrijskih procesih.