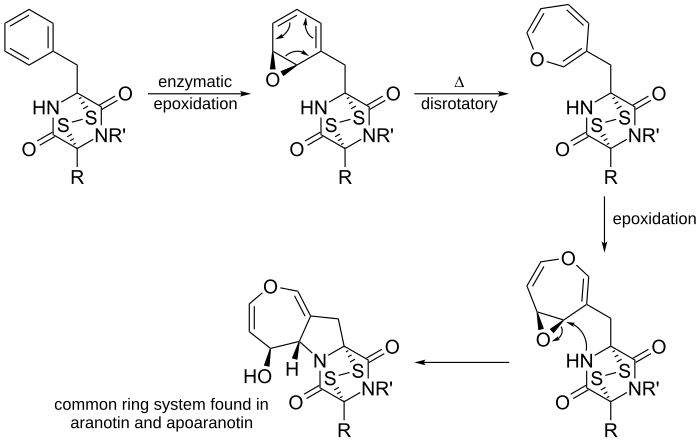
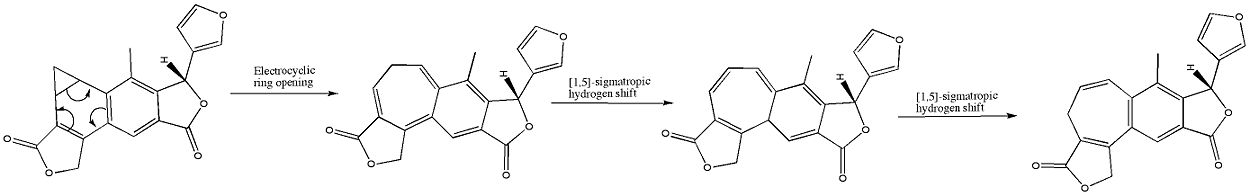
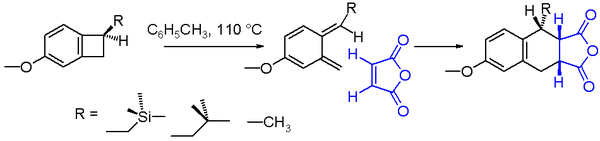
V organski kemiji je elektrociklična reakcija posebna vrsta periciklične reakcije preureditve, pri kateri se v eni concertirani (enostopenjski) preureditvi spremeni ena vez pi v eno vez sigma (zapiranje obroča) ali obratno, ena vez sigma v vez pi (odpiranje obroča). Elektrociklične reakcije imajo več skupnih značilnosti:
- lahko so spodbudjene s svetlobo (fotoinducirane) ali s toploto (termične); način poteka (konrotatorno ali disrotatorno) je odvisen od stanja (ground ali excited)
- način reakcije je odvisen od števila π elektronov v konjugiranem sistemu; pomembno je, ali gre za sistem z 4n ali 4n+2 π elektroni
- reakcija lahko zapre obroč (elektrociklizacija) ali odpre obroč (elektrociklično odpiranje)
- stereospecifičnost je določena s konrotatorno ali disrotatorno tvorbo prehodnega stanja, kot to napovedujejo Woodward-Hoffmannova pravila
Osnovni mehanizem in pravila izbire poti
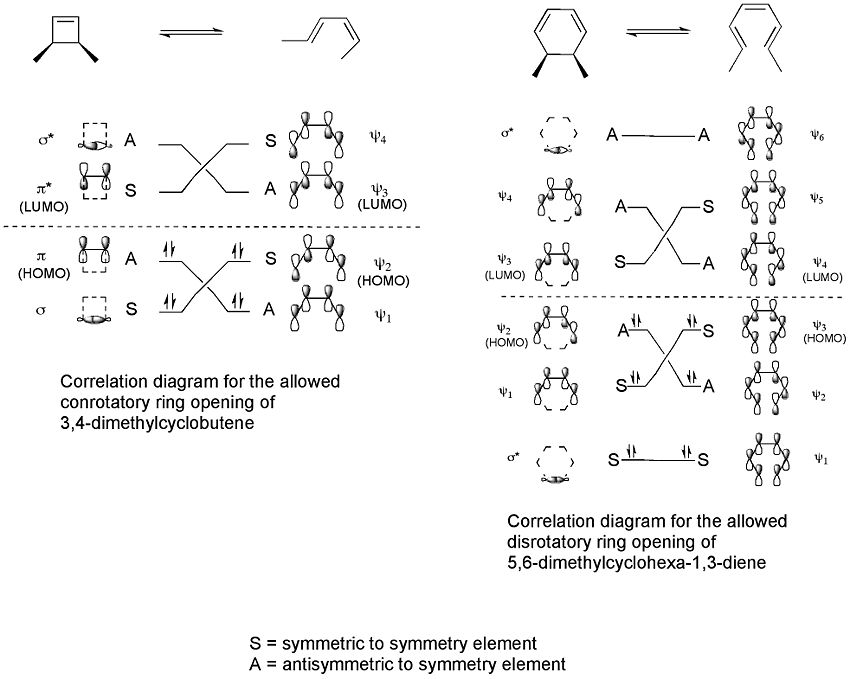
Elektrociklične reakcije potekajo concertirano skozi ciklično prehodno stanje, pri čemer so ključne simetrijske lastnosti molekulske orbitalne porazdelitve. Woodward-Hoffmannova pravila dajejo preprosto pravilo, katera stereokemijska pot bo termično in katera fotokemično favorizirana:
- Za sisteme z 4n π elektroni (n = 1, 2, ...): termično poteka konrotatorno, fotokemično pa disrotatorno.
- Za sisteme z 4n+2 π elektroni (n = 0, 1, ...): termično poteka disrotatorno, fotokemično pa konrotatorno.
To pomeni, da je odločilen HOMO reagenta (pri termični reakciji) oziroma orbitali v fotokemijskem ekscitiranem stanju: pri zapiranju obroča morajo p-orbitale vzdolž konjugiranega sistema poravnati faze tako, da se lahko tvorijo ali prekinjajo σ vezi brez kršitve ohranitve simetrije orbit.
Metoda mejnih orbital (FMO) in primeri
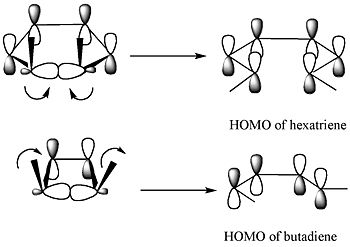
Metoda mejne orbite (frontier molecular orbital, FMO) pojasni, zakaj določena smer rotacije (konrotatorna ali disrotatorna) vodi do produkta z ustrezno simetrijo. Pri termičnem odpiranju ciklobutenov (4 π elektronov) se σ vez odpira tako, da nastale p-orbitale ohranijo fazno ujemanje HOMO produkta (butadiena). To je mogoče le s konrotatornim odpiranjem obroča, medtem ko bi disrotatorno odpiranje dalo nezdružljive faze in zato neproduktivno pot.
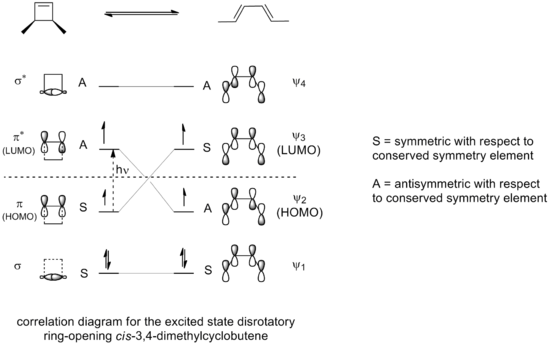
Tipičen primer je termična reakcija obročnega odpiranja 3,4-dimetilciklobutena. Cis-izomer daje izključno cis,trans-2,4-heksadien, medtem ko trans-izomer daje trans,trans-dien. Slika prikazuje potek in stereokemijo:
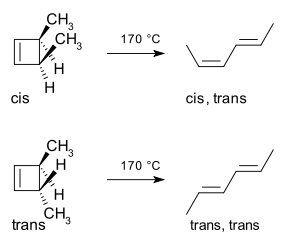
Diagram mejnih orbital, ki prikazuje faze lobusov in zahtevo po konrotatornem odpiranju v tem primeru, je prikazan spodaj:
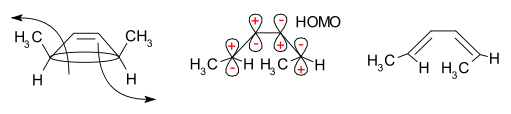
Torkoselektivnost (torquoselectivity) in stereokontrol
Torkoselektivnost se nanaša na preferenčno smer vrtenja (»torque«) substituentov med elektrocikličnim zapiranjem ali odpiranjem. Čeprav je splošna metoda (konrotatorno/disrotatorno) določena z orbitalno simetrijo, lahko dodatni dejavniki — sterični vplivi, elektronski učinki substituentov, koordinacija s kovinskimi kationi ali kompleksacija z Lewisovimi kislinami — favorizirajo eno smer vrtenja nad drugo. Posledica je lahko enantioselektivnost (enantiomerni presežek) ali diastereoselektivnost produkta.
Pri konrotatorni reakciji imajo substituenti še vedno možnost vrtenja v levo ali desno; če noben vpliv ne preferira smeri, se tvori racemična mešanica enantiomerov. Če pa nek dejavnik omeji eno smer vrtenja (delno ali popolnoma), nastane enantiomerni presežek produkta. Takšno nadzorovanje torkoselektivnosti se uporablja v sintetični kemiji za pridobivanje posameznih stereoizomerov.
Pomembne reakcije in aplikacije
Nazarova reakcija ciklizacije je praktičen primer elektrociklične elektrociklizacije, pri kateri se divinilketoni pretvorijo v ciklopentenone; to je pomembna metoda za gradnjo cikličnih struktur v organski sintezi. (Odkril jo je Ivan Nikolajevič Nazarov (1906–1957).)
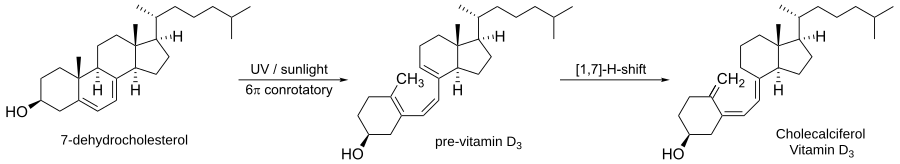
Drugi primeri vključujejo elektrocilizacijo heksatriena v cikloheksadien (6 π sistem) in različne fotokemijske elektrociklične reakcije, ki se uporabljajo pri pripravi poličnih naravnih produktov in kompleksnih cikličnih ogljikovih ogrodij. Elektrociklične reakcije so tudi temelj nekaterih procesov v materialih in fotokemiji, kjer se s svetlobo krmilijo spremembe konjugacije in oblikovanja obročev.
Zaključek in eksperimentalni dokazi
Kemike zanimajo elektrociklične reakcije, ker eksperimentalni rezultati pogosto potrjujejo teoretične napovedi ohranitve simetrije molekulskih orbital in ohranitev njihovega zaporedja. Spektralni podatki, stereokemijska analiza produktov in študije z oznakami (labeling) dajejo neposredne dokaze za concertiran mehanizem in napovedano stereospecifičnost.
V praksi se izbira termalnega ali fotokemičnega pogoja ter uvedba katalizatorjev ali koordinacijskih partnerjev uporablja kot orodje za nadzor stereokemije in torkoselektivnosti, kar omogoča natančno načrtovanje sintez kompleksnih molekul.
Več o stereokemiji elektrocikličnih reakcij in praktičnih primerih najdete v specializirani literaturi ter v izvornih člankih o Woodward–Hoffmannovih pravilih in o konkretnih reakcijah, kot je Nazarova ciklizacija.