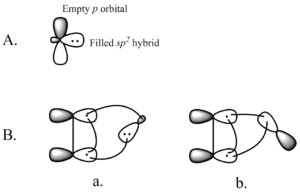
Cheletropske reakcije so vrsta pericikličnih reakcij, pri katerih en atom na enem od reagentov dobi dve novi vezi. Periciklična reakcija je reakcija, ki vključuje prehodno stanje s cikličnim nizom atomov in s tem povezanim cikličnim nizom interakcijskih orbital. V tem cikličnem polju pride do reorganizacije vezi σ in π.
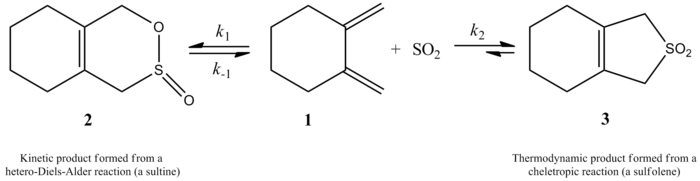
Cheletropske reakcije so podrazred cikloadicij. Cheletropske reakcije se razlikujejo po tem, da se pri enem od reagentov obe novi vezi tvorita na isti atom. Nekaj primerov je prikazanih na desni strani slike 1. V prvem primeru je edini atom ogljikov atom v karbonilni skupini. Ta ogljikov atom se konča v ogljikovem monoksidu. Končni rezultat je vzpostavitev dveh novih vezi z enim atomom. Prva dva primera sta znana kot "cheletropna iztisnitev", ker se pri reakciji izloči majhna stabilna molekula. Pogonska sila teh reakcij je pogosto entropična korist od sproščanja plina (npr. CO ali N2).
Definicija in osnovni principi
Cheletropska reakcija je periciklična cikloadicija, pri kateri nastaneta dve novi vezi, vendar sta obe vezani na isti atom v enem od reaktantov. Prehodno stanje je ciklično in reakcija poteka koordinirano — to pomeni, da poteka brez vmesnih, daljših radikalnih ali ionskih stopinj, kadar gre za koncertedni potek. Najpogosteje gre za interakcijo med večnatomskim π-sistemom in monovalentnim centrom (npr. karben, atom žvepla ali ogljika z več vezmi).
Mehanizem in orbitalna simetrija
Ker so cheletropske reakcije periciklične, jih urejajo pravila o ohranitvi orbitalne simetrije (Woodward–Hoffmann). Pomembno je naslednje:
- Prehodno stanje vključuje zaprt krog interakcijskih orbital (σ in π), zato je možno le, če so faze in simetrija ujemajoče.
- Termalno ali fotokemično dovoljenje: glede na število vključenih elektronov in način pristopa (suprafacialno ali antarafacialno) lahko določena cheletropska reakcija poteka termalno ali pa zahteva fotonsko ekscitacijo.
- Stereospecificnost: ko reagira singlet karben ali drug reagenta s parno konfiguracijo orbital, je potek pogosto concerted in stereospecifičen — na primer stereokemija alkena se prenese v produkt (cis → cis, trans → trans pri ciklopropanizaciji).
Stereokemija in vpliv reaktivnega centra
Vrsta reaktivnega centra (npr. singlet ali triplet karben) močno vpliva na mehanizem in stereokemijo:
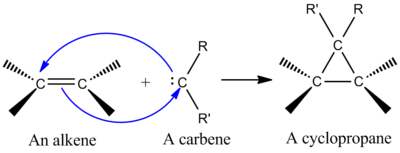
- Singlet karbeni (npr. :CH2, :CCl2) običajno reagirajo concertedno in cheletropno, kar daje stereospecifične produkte — ciklopropani z ohranjeno stereokemijo iz izhodiščnega alkena.
- Triplet karbeni pogosto reagirajo preko radikalnih, stopnjami posredovanih poti, kar lahko vodi do izgube stereospecifičnosti ali do radikalnih stranskih produktov.
- V primeru heteroatomov (S, N, O) ali delcev z neparnimi elektroni so možni kompleksnejši poteki z delokalizacijo nabojev in alternativnimi prehodnimi stanji.
Tipični primeri
- Ciklopropanizacija alkenov s karbeni: dodatek karbenov (npr. metilenski :CH2 ali dichlorokarben :CCl2) na dvojno vez je klasičen primer cheletropske reakcije — nastane ciklopropan, pri katerem sta obe novi vezi vezani na isti ogljikov atom karbena.
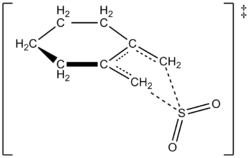
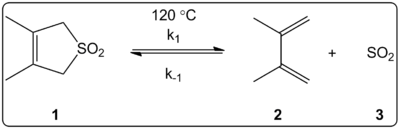
- Dodatek žvepla(IV) dioksida (SO2) na diene: reakcija 1,3-dienov z SO2 lahko poteka kot cheletropska adicija in tvori sulfolene ali sorodne produkte; ta proces se uporablja tudi v sintezi in kot reverzibilna pot (izločanje SO2).
- Cheletropne iztisnitve: obrat cheletropske adicije, kjer se izloči majhna molekula (npr. CO, N2, SO2), velja za pogost mehanizem, ki ga poganje entropična korist in stabilnost izločenega plina.
Pogoji reakcije in praktični pomen
Cheletropske reakcije se lahko sprožijo termično ali fotokemično glede na simetrijo vključenih orbital. V praksi so pomembne v organski sintezi zaradi naslednjih razlogov:
- Omogočajo hitro oblikovanje dveh vezi na enem centru (npr. pri ciklopropanizaciji), kar je uporabno pri pripravi obročnatih struktur.
- Cheletropne iztisnitve (izločanje majhnih molekul) se uporabljajo kot pogonski korak v zaporedjih reakcij za pridobivanje aromatskih ali zmanjšanih struktur.
- Razumevanje orbitalne simetrije omogoča nadzor nad stereokemijo produkta in izbiro ustreznih pogojev (termalno vs fotokemično).
Povezava do teorije in eksperimenta
Za pravilno načrtovanje in razlago cheletropskih reakcij so koristni računalniški izračuni (DFT), študije prehodnih stanj in eksperimenti s stereokemijo (npr. uporaba označenih substratov). V eksperimentalnem delu se poleg karbenov pogosto uporabljajo reagentni sistemi, ki generirajo reaktivne enote in omogočajo selektivno cheletropno adicijo ali iztisnitev.
Zaključek
Cheletropske reakcije so specifičen, a pomemben podrazred pericikličnih procesov, kjer en atom tvori hkrati dve vezi. Njihova concerted narava, odvisnost od orbitalne simetrije in praktična uporabnost v organski sintezi jih naredijo za koristen koncept tako v teoriji kot v laboratoriju. Posebej so uporabne pri ciklopropanizacijah, tvorbi heterocikličnih struktur in v postopkih, kjer se z izločitvijo majhne molekule doseže termodinamična prednost.
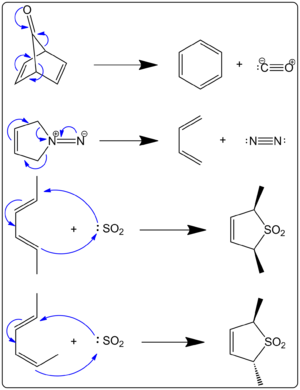

![{\displaystyle {\frac {d[3]}{dt}}=k_{2}[1][SO_{2}]^{2}}](https://www.alegsaonline.com/image/a02f69dd0783356fbf24499f57d0df29cd264f16.svg)