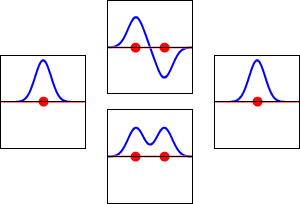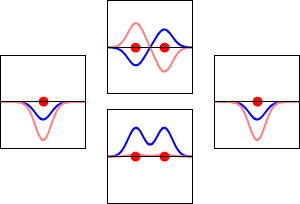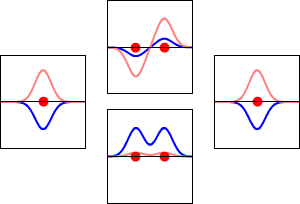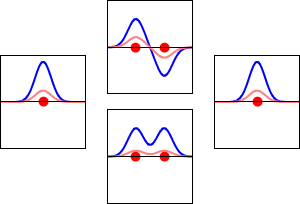
V kemiji molekulska orbitala (ali MO) pojasnjuje, kaj se zgodi z elektroni, ko se atomi združijo v molekulo. MO je matematična funkcija, ki opisuje valovno obnašanje elektrona v molekuli. Kemiki take funkcije uporabljajo za napovedovanje ali razlago kemijskih in fizikalnih lastnosti. Funkcije lahko na primer povedo, kakšna je verjetnost, da najdemo elektron na določenem območju.
Kemiki matematične modele molekulskih orbital običajno zgradijo s kombiniranjem atomskih orbital. Uporabijo se lahko tudi hibridne orbitale iz vsakega atoma molekule ali druge molekulske orbitale iz skupin atomov. Na teh funkcijah lahko delajo računalniki. Molekularne orbitale omogočajo kemikom uporabo kvantne mehanike pri preučevanju molekul. MO odgovarjajo na vprašanja o tem, kako se atomi v molekulah držijo skupaj. Različne zaokrožene oblike v orbitalnem diagramu označujejo, kje v atomu bi se najverjetneje nahajali elektroni.
Kako nastanejo molekulske orbite
Molekulske orbitale nastanejo, ko se atomske orbitale posameznih atomov kombinirajo. Najpogostejši pristop je linearna kombinacija atomskih orbital (LCAO), pri katerem se valovne funkcije atomov seštevajo ali odštevajo. Če se valovni funkciji pri seštevanju fazi ujemata, dobimo vezujočo (bonding) orbitalo z nižjo energijo. Če pa se valovni funkciji izničita (ničelna interferenca), nastane antivezujoča (antibonding) orbitala z višjo energijo.
Vrste orbital glede na simetrijo
- Sigma (σ): nastane z vzdolžnim prekrivanjem orbital ob osi vezi (npr. 1s–1s ali 2p_z–2p_z). Ima rotacijsko simetrijo okoli osi vezi.
- Pi (π): nastane z bočnim prekrivanjem p-orbital; ima vozlične ravnine in eno vozliščno ravnino skozi os vezi.
- Delta (δ) in druge: pri prekrivanju kompleksnih d-orbital lahko nastanejo še redkejše simetrije.
Energije, zasedenost in bond order
V molekuli so MO porazdeljene po energiji. Elektroni zapolnijo orbitale od najnižje energije navzgor (način, podoben zapolnjevanju atomskih orbital). Pomembna sta pojma HOMO (Highest Occupied Molecular Orbital) in LUMO (Lowest Unoccupied Molecular Orbital) — razliko med njima pogosto imenujemo tudi energijski pas ali režo, pomembno pri absorpciji svetlobe in reaktivnosti.
Bond order (ničelna doza vezi) lahko ocenimo kot (število elektronov v vezujočih MO − število elektronov v antivezujočih MO) / 2. Višji bond order pomeni močnejšo vez.
Primeri in posledice
- H2: dve 1s atomski orbitali se kombinirata v eno vezi vezujočo σ in eno antivezujočo σ*. Ob dveh elektronih v σ je molekula stabilna.
- O2: konfiguracija MO razloži paramagnetizem kisika — v π* (antivezujočih) orbitalah so dva neusklajena (neparna) elektrona, zato je O2 paramagneten.
- Benzenski π-sistem: šest p-orbital se delokalizira v šest π MO, kar vodi v energijsko stabilizacijo (aromatičnost) in enakomerno delitev vezi.
Vloga pri kemijski reaktivnosti
Frontier orbital teorija poudarja pomen HOMO in LUMO pri reakcijah: nukleofilne vrste pogosto darujejo elektrone iz svojega HOMO, elektrofili pa sprejemajo elektrone v svoj LUMO. Ujemanje energij in prostorskega premikanja teh orbital določa, ali bo jedro interakcije hitro in selektivno.
Vizualizacija in vozlišča
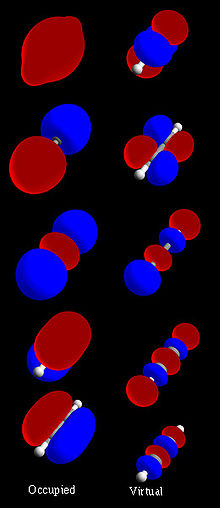
Molekulske orbitale lahko prikažemo kot površine, kjer je verjetnost najdbe elektrona določena z gostoto v tej površini. Vozlišča so regije, kjer je valovna funkcija enaka nič — antivezujoče orbitale imajo več vozlišč in višjo energijo. Barvna označba običajno prikazuje fazo (pozitivno/negativno) valovne funkcije.
Računalniške metode
Za izračun in risanje MO se uporabljajo metode kvantne kemije, npr. Hartree–Fock (HF), teorija funkcionala gostote (DFT), ter naprednejše metode, kot so konfiguracijska interakcija (CI) ali Coupled Cluster (CC). Računalniški izračuni omogočajo napoved geometrije, energij, spektrov in reaktivnosti.
Povezava z eksperimentalnimi opazovanji
Molekulske orbitale neposredno vplivajo na spektre (UV–Vis, fotoelektronska spektroskopija), elektronske lastnosti in magnetne lastnosti. Prehodi med MO (npr. HOMO → LUMO) povzročijo absorpcijo svetlobe, kar je osnova za barve in fotokemijo.
Kaj si zapomniti
- Molekulska orbitala opisuje verjetnostno porazdelitev elektrona v molekuli.
- Vezujoče orbitale znižujejo energijo in stabilizirajo molekulo; antivezujoče jo zvišujejo.
- HOMO in LUMO sta ključna za razumevanje reaktivnosti in spektrov.
- Računalniške metode omogočajo natančne modele MO ter razlago eksperimentalnih podatkov.
Ta pregled predstavlja osnovne koncepte molekulskih orbital. Za poglobljeno razlago specifičnih primerov (npr. gradnja MO-diagrama za določeno molekulo) je priporočljivo pogledati konkretne risbe orbital in izračune za izbrano molekulo.