Encimi so beljakovinske molekule v celicah, ki delujejo kot biološki katalizatorji. Encimi pospešujejo kemične reakcije v telesu, vendar se pri tem ne porabijo, zato se lahko vedno znova uporabljajo. Skoraj vse biokemične reakcije v živih bitjih potrebujejo encime; z encimom potekajo reakcije veliko hitreje, kot bi potekale brez njega. Obstajajo tudi encimom podobni biokatalizatorji iz RNK, imenovani ribocimi, ki imajo vlogo v nekaterih procesih (npr. samorepliciranje nekaterih molekul RNK).
Kaj so substrati in produkti
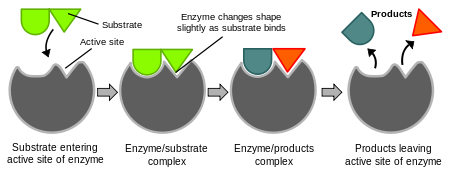
Snovi na začetku reakcije imenujemo substrati. Snovi na koncu reakcije so produkti. Encimi delujejo na substrate in jih spreminjajo v produkte z znižanjem aktivacijske energije reakcije. Študij encimov se imenuje encimologija.
Kako encimi delujejo
Encimi imajo posebno mesto za vezavo substrata, imenovano aktivno mesto. Ko se substrat veže, encim pogosto spremeni obliko (model induced fit), kar pomaga pravilni orientaciji substrata in olajša prehodno stanje reakcije. Mehanizmi, ki jih encimi uporabljajo, vključujejo zbliževanje reaktantov, destabilizacijo vezi v substratu, prenos protonov ali elektronov ter začasno tvorbo kovalentnih vezi s substratom.
Struktura in specifičnost
Večina encimov je iz polipeptidnih verig (beljakovin), katerih tridimenzionalna struktura določa funkcijo. Specifičnost encima pomeni, da bo določen encim prepoznal in obdelal le enega ali malo število sorodnih substratov — zato imajo encimi vlogo natančnih "kemijskih orodij". Nekateri encimi pa so splošneje delujoči in sprejmejo več različnih substratov.
Cofaktorji in koencimi
Mnogo encimov potrebuje dodatne nenavidezne komponentne za delovanje. Ti so lahko kovinski ioni (npr. Zn2+, Mg2+, Fe2+) ali organske molekule, imenovane koencimi (npr. NAD+, FAD, koencim A). Koencimi prenašajo kemične skupine ali elektrone med reakcijami in so pogosto obnovljeni v drugih reakcijah.
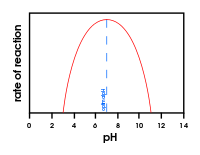
Dejavniki, ki vplivajo na aktivnost
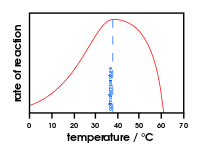
- Temperatura: z naraščanjem temperature aktivnost običajno narašča do optimalne vrednosti; pri previsoki temperaturi se encim denaturira in aktivnost izgine.
- pH: encimi imajo optimalno pH, pri katerem delujejo najbolje; odstopanja spreminjajo ionizacijo strukturnih skupin in zmanjšajo učinkovitost.
- Koncentracija substrata in encima: pri nizkih koncentracijah substrata se hitrost povečuje sorazmerno; pri visokih koncentracijah pride do nasičenja aktivnih mest (model Michaelisa–Menten).
- Inhibitorji in aktivatorji: prisotnost inhibitorjev lahko zmanjša aktivnost encima, aktivatorji pa jo lahko povečajo.
Vrste inhibitorjev
Najpogostejše razlike so:
- Konkurentni inhibitorji: tekmujejo s substratom za aktivno mesto; vpliv lahko omilimo z višjo koncentracijo substrata.
- Nekonkurentni inhibitorji: se vežejo na drug del encima in spreminjajo njegovo aktivnost ne glede na koncentracijo substrata.
- Mešani in nepravi inhibitorji: imajo lastnosti obeh zgornjih tipov.
Biološka in medicinska pomembnost
Encimi so ključni za prebavo (npr. amilaze, proteaze, lipaze), presnovo (npr. kinaze in dehidrogenaze), podvajanje DNK (DNA polimeraze), celično dihanje (npr. citokromi in ATP sintaza) in številne druge procese. Pomanjkanje ali nepravilno delovanje določenih encimov povzroči dedne bolezni (npr. fenilketonurija zaradi pomanjkanja fenilalanin hidroksilaze). Encimi so tudi pomembni biomarkerji v diagnostiki (npr. povišane transaminaze pri poškodbi jeter).
Farmakologija in nadzor
Veliko zdravil deluje kot encimski inhibitorji (npr. statini zavirajo HMG-CoA reduktazo, ACE inhibitorji vplivajo na encim, ki uravnava krvni tlak). Razumevanje delovanja encimov je zato ključno za razvoj zdravil in terapij.
Industrijska uporaba in biotehnologija
Encimi se široko uporabljajo v industriji: v pralnih praških (proteaze, amilaze), pri proizvodnji hrane in pijač (encimi za fermentacijo, za izboljšanje kruha, za razgradnjo škroba), pri obdelavi tekstila, v papirni industriji in v proizvodnji biogoriv. Encimsko inženirstvo in usmerjena evolucija omogočata prilagajanje encimov za specifične industrijske pogoje (npr. stabilnost pri visokih temperaturah).
Merjenje aktivnosti in enote
Encimsko aktivnost merimo s spremljanjem pretoka substrata v produkt v časovni enoti. Pogoste enote so katal (kat) in enota aktivnosti (U), kjer 1 U = količina encima, ki katalizira pretvorbo 1 μmol substrata na minuto pod določenimi pogoji.
Kratek zgodovinski pregled
Prvi encim, diastazo (kasneje imenovano amilaza), je leta 1833 odkril Anselme Payen. Od takrat je področje encimologije napredovalo do molekularnega razumevanja mehanizmov, struktur in regulacije, kar omogoča uporabo encimov v biologiji, medicini in industriji.
Encimi so torej osnovni gradnik življenja: omogočajo hitre, kontrolirane in učinkovite biokemične reakcije, brez katerih življenje ne bi bilo mogoče.