Sigmatropna reakcija v organski kemiji je ena izmed oblik pericikličnih reakcij. Gre za intramolekularen, običajno nekataliziran proces, pri katerem se ena σ-vezava spremeni v drugo σ-vezavo znotraj iste molekule. Ime sigmatropna reakcija izhaja iz besede "sigma" za enojne vezi (ogljik–ogljik) in grške besede tropos (obrat), kar opisuje premik substituenta ali σ‑vezi med deli sistema π, medtem ko se sistem π hkrati preuredi. To je preureditvena reakcija (reakcija preureditve) — atomi se navadno ne odstranijo in ne dodajo novih — in v pravih sigmatropnih procesih običajno ni potrebna zunanja kataliza. Nekatere sigmatropne reakcije pa lahko pospešijo Lewisove kisline ali prehodne kovine, ki tvorijo vmesne produkte in omogočijo alternativne mehanizme. Najbolj znane sigmatropne preureditve so [3,3] Copejeva preureditev, Claisenova preureditev, Carrollova preureditev in Fischerjeva indolna sinteza.
Mehanizem
Sigmatropne reakcije so običajno concertedne in potekajo preko pericikličnega prehoda s krožno porazdelitvijo elektronov v tranzicijskem stanju. Pri tej concertedni preureditvi se σ-elektroni "selijo" vzdolž π-sistema, kar vodi do nove σ‑veze. V mnogih primerih je tranzicijsko stanje aromatskega tipa (Hückelova ali Möbiusova aromatičnost v prehodnem stanju), kar stabilizira prehodno stanje in omogoči reakcijo.
V praksi pa se lahko mehanizem odkloni od popolnoma concertednega: v prisotnosti močnih kataliz, radikalnih ali ionskih pogojev ali prehodnih kovin se lahko pojavijo vmesne stopnje z radikali ali ionskimi kompleksi, kar spremeni kinetiko in selektivnost reakcije.
Vrste sigmatropnih preureditev
- Po velikosti premika: označene kot [i,j] (npr. [1,3], [1,5], [3,3]), kjer i in j predstavljata število vezi/atomov po vsaki strani systema, preko katerega se σ‑veza premakne.
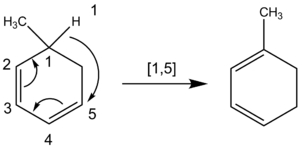
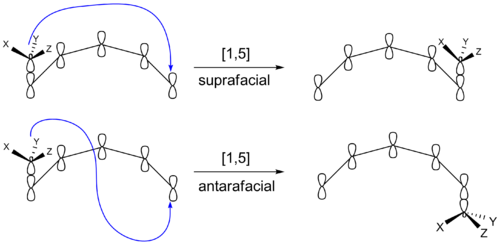
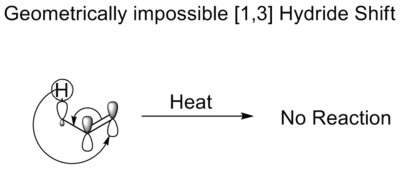
- Premiki vodika: npr. [1,5]-H premik je običajno termično dovoljen in pogosto poteka suprafacialno; [1,3]-H premik je večinoma termično prepovedan in zahteva visoke energije ali fotonsko iniciacijo.
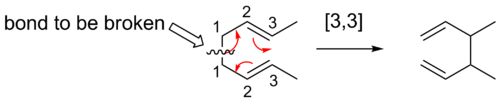
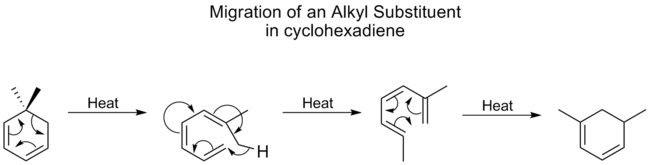
- Carbon‑premiki: npr. [3,3]-preureditve (Claisen, Cope) so zelo pogoste v sintezi in potekajo skozi stabilna tranzicijska stanja.
- Inter- vs intramolekularno: osnovna definicija se nanaša na intramolekularne procese; obstajajo pa tudi interciklični ali bimolekularni analogi, ki vključujejo posredovanje kataliz.
Stereokemija in Woodward–Hoffmann pravila
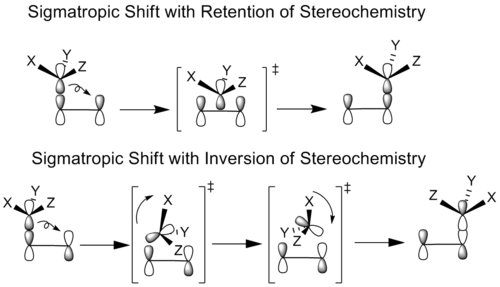
Uporaba Woodward–Hoffmann pravil omogoča napovedovanje, ali bo sigmatropna preureditev termično ali fotokemično dovoljena kot suprafacialna ali antarafacialna premestitev. Na kratko:
- Suprafacialno pomeni, da se skupina premakne po isti strani π‑sistema.
- Antarafacialno pomeni, da se premik izvede po nasprotnih straneh π‑sistema (pogosteje sterično oteženo in zato redkeje).
- Termično so običajno dovoljeni prehodi, ki vključujejo (4n+2) π‑elektronov suprafacialno, medtem ko lahko fotonska ekscitacija spremeni pravila in omogoči fotokemično dovoljene poti, ki so termično prepovedane.
Primeri
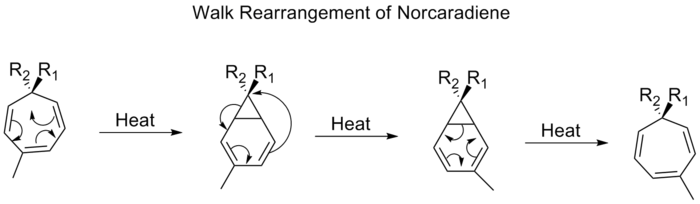
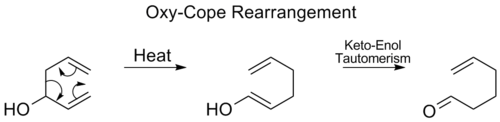
- Copejeva preureditev ([3,3]): en klasičen primer sigmatropne preureditve, kjer se C–C in C=C vezi preuredijo v konjugiranem 1,5‑dienu. Pogosta v termični preureditev alicin‑podobnih sistemov.
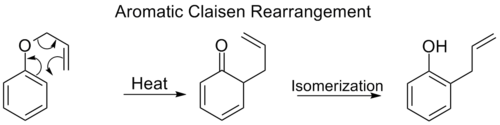
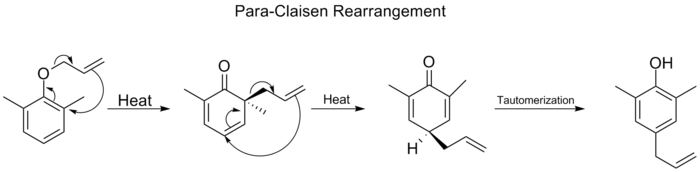
- Claisenova preureditev ([3,3]): preureditev alil vinil etrov v γ,δ‑nenasičene karbonilne sisteme; zelo uporabna v organski sintezi za oblikovanje C–C vezi in kontrolirano nastavljanje konfiguracije.
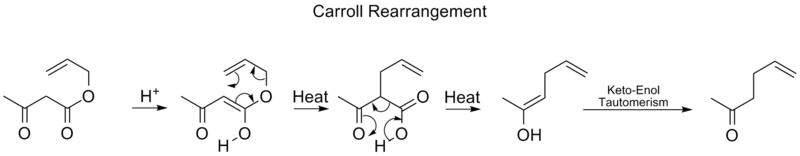
- Carrollova preureditev: povezana z decarboxilativnimi [3,3] preureditevmi v sintezi c‑alkenilov.
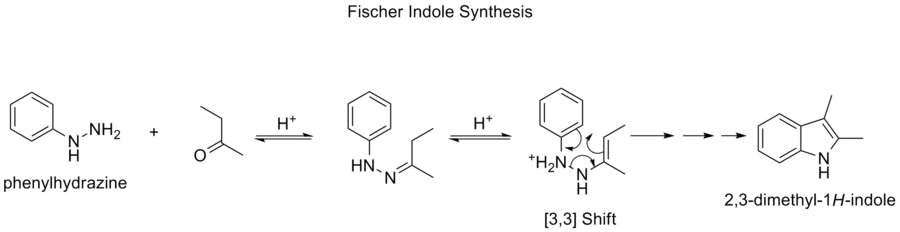
- Fischerjeva indolna sinteza: klasična metoda za tvorbo indolskih jeder, ki vključuje več korakov, med katerimi se pojavi sigmatropna preureditev kot eden ključnih korakov reorganizacije.
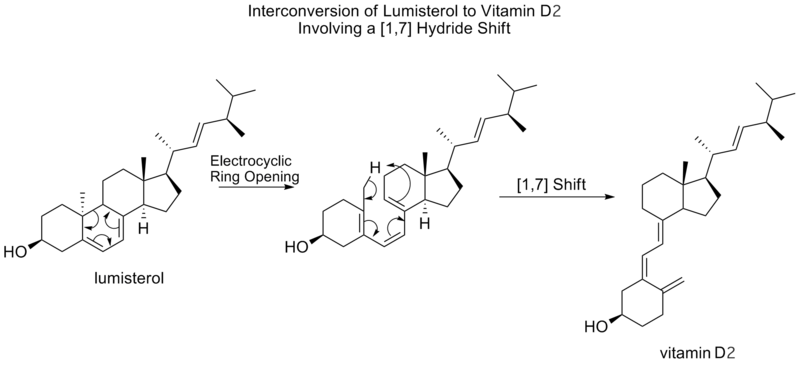
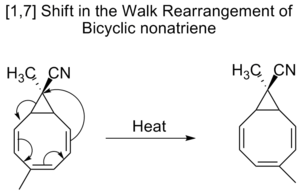
- H‑premiki: [1,5]-H premiki so pogosto hitri pri primernih sistemih (npr. konjugirani dieni) in se uporabljajo pri izomerizacijah; [1,3]-H premiki so običajno počasni in termično neugodnejši.
Kataliza in odstopanja od concertednega mehanizma
Čeprav so sigmatropne reakcije načeloma nekatalizirane in concertedne, lahko Lewisove kisline ali kompleksi prehodnih kovin stabilizirajo vmesne strukture, spremenijo energijske profile ali celo odprejo alternativne, stopnjevane mehanizme. Takšni pogoji se pogosto uporabljajo za znižanje aktivacijskih energij ali doseganje drugačne selektivnosti v sintetičnih aplikacijah.
Pomen v organski sintezi
Sigmatropne preureditev so dragocene pri gradnji kompleksnih ogljikovih ogrodij, premikanju substituentov na predvidljiva mesta in v oblikovanju stereokemije produktov. Zaradi svoje concertedne narave pogosto zagotavljajo visoko stereospecifičnost in čistost produktov, kar je koristno pri sintezi naravnih produktov in farmacevtskih molekul.
Zaključek
Sigmatropne reakcije predstavljajo pomembno podskupino pericikličnih reakcij z značilnim prehodom σ‑vezi vzdolž π‑sistema. Razumevanje njihovih mehanizmov, stereokemije in pogojev (toplotno vs fotokemično, suprafacialno vs antarafacialno) omogoča načrtovanje učinkovitih strateških potez v organski sintezi ter uporabo teh preureditev v naprednih metodah priprave kompleksnih molekul.

![[1,3] Alkyl Shifts](https://www.alegsaonline.com/image/550px-1,3alkylfixed.png)
![[1,5] Hydride shift in a cyclic system](https://www.alegsaonline.com/image/300px-1,5hydridecyclicfixed.png)
![Antarafacial [1,5] Hydride Shift](https://www.alegsaonline.com/image/600px-1,5hantarafacialfixed.png)


![[5,5] shift of phenyl pentadienyl ether](https://www.alegsaonline.com/image/800px-5,5shiftfixeds.png)